
分析 (1)①Na2S水解呈碱性,且有两步水解,以第一步水解为主;
②A.Na2S的水解程度比NaHS大;
B.根据水解方程和电离方程可知两溶液中含有的离子种类相同;
C.两溶液中滴入同体积同浓度的盐酸,NaHS产生气体速率快;
D.两溶液中加入NaOH固体,水解平衡逆移,c(S2-)都增大
E.NaHS溶液显碱性,以水解为主;
(2)根据溶度积常数计算$\frac{c(B{r}^{-})}{c(C{l}^{-})}$;
(3)利用盖斯定律计算反应热;
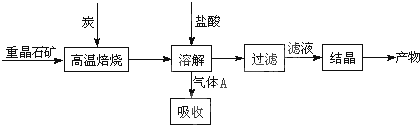
(4)加入过量C可提高冰晶石的转化率,同时维持反应进行.
解答 解:(1)①Na2S为强碱弱酸盐,水解呈碱性,且有两步水解,以第一步水解为主,第一步水解生成离子HS-,第二步水解生成H2S,水解的离子方程式分别为S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH-,
故答案为:S2-+H2O?HS-+OH-; HS-+H2O?H2S+OH-;
②A.Na2S的水解程度比NaHS大,所以Na2S溶液的pH比NaHS溶液pH大,故A错误;
B.根据水解方程S2-+H2O?HS-+OH-; HS-+H2O?H2S+OH-;和电离方程HS-?S2-+H+;可知两溶液中含有的离子种类相同,故B错误;
C.两溶液中滴入同体积同浓度的盐酸,Na2S+HCl=NaHS+NaCl;NaHS+HCl=H2S↑+NaCl;所以NaHS产生气体速率快,故C错误;
D.两溶液中加入NaOH固体,水解平衡逆移,c(S2-)都增大,故D正确;
E.NaHS溶液显碱性,以水解为主,c(OH-)>c(H+),所以c(Na+)>c(HS-)>c(OH-)>c (H+)>c(S2-),故E正确;
故答案为:D、E;
(2)当两种沉淀共存时,Ag+离子浓度相同,根据溶度积常数计算,c(Br-)=$\frac{{K}_{SP}(AgBr)}{C(A{g}^{+})}$,c(Cl-)=$\frac{{K}_{SP}(AgCl)}{C(A{g}^{+})}$,则$\frac{C(B{r}^{-})}{C(C{l}^{-})}$=$\frac{5.4×1{0}^{-13}}{2.0×1{0}^{-10}}$=2.7×10-3.
故答案为:2.7×10-3;
(3)利用盖斯定律求解:
BaSO4(s)+4C(s)$\frac{\underline{\;高温\;}}{\;}$4CO(g)+BaS(s)△H1=571.2kJ•mol-1 ①
BaSO4(s)+2C(s)$\frac{\underline{\;高温\;}}{\;}$2CO2(g)+BaS(s)△H2=226.2kJ•mol-1 ②
将以上两个热化学方程式相减,然后除以2可得:
C(s)+CO2(g)$\frac{\underline{\;高温\;}}{\;}$2CO(g)△H=$\frac{571.2KJ/mol-226.2KJ/mol}{2}$=+172.5kJ•mol-1,
故答案为:+172.5KJ/mol;
(4)加入过量C可提高冰晶石的转化率,以上反应为吸热反应,炭和氧气反应放热维持反应所需高温,
故答案为:使BaSO4得到充分的还原(或提高BaS的产量),①②为吸热反应,炭和氧气反应放热维持反应所需高温.
点评 本题考查较为综合,题目具有一定难度,涉及盐类的水解、难溶电解质的溶解平衡、反应热的计算等问题,本题注意溶度积常数的利用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe3+ | B. | Cr2O${\;}_{7}^{2-}$ | C. | Br2 | D. | HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
 和
和 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
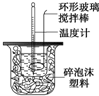 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在上图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在上图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 30.6 | 5.5 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y分别与X、Z形成的化合物中化学键类型相同 | |
| B. | 原子半径的大小顺序:r(Z)>r(W)>r(Y) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | Z的最高价氧化物对应的水化物是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2项 | B. | 3项 | C. | 4项 | D. | 5项 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com