
| A. | 可燃冰是一种天然气的水合物,它的开采使用有助于解决温室效应 | |
| B. | 天然食品添加剂比化学合成品安全可靠 | |
| C. | 有一种新发现的固态碳,称为“纳米泡沫”,外形似海绵,密度小,有磁性,这种碳与金刚石的关系是同素异形体 | |
| D. | 工业酒精含95%左右的乙醇,可以用于酒精饮料的勾兑,降低生产成本 |
分析 A.天然气的成分是甲烷;
B.化学合成品添加剂安全性在合成时已充分考虑,而天然食品添加剂中有毒的物质无法去除;
C.同一元素形成的不同单质互称同素异形体;
D.工业酒精中含有甲醇.
解答 解:A.天然气的成分是甲烷,甲烷也是一种产生温室效应的一种气体,故A错误;
B.许多天然食品添加剂成分复杂,由于分离、检测技术限制,某些不安全成分可能并没有被识别和去除,化学合成品添加剂确定了其安全性,故B错误;
C.纳米泡沫碳与金刚石都是碳元素形成的不同单质,所以互为同素异形体,故C正确;
D.工业酒精中含有甲醇,甲醇有剧毒,不能用于酒精饮料的勾兑,故D错误.
故选C.
点评 本题考查化石燃料与基本化工原料,难度不大,注意工业酒精中含有甲醇,甲醇有剧毒,不能用于酒精饮料的勾兑.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子序数X>Y | B. | 最外层电子数X>Y | C. | 原子半径X<Y | D. | 最高正价X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
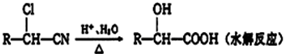
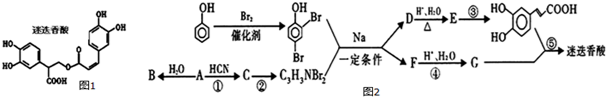
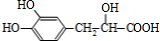 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$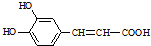 +H2O
+H2O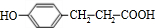 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| B. | 过氧化钠与水反应时,每生成0.1mol氧气转移的电子数为0.4NA | |
| C. | 电解精炼铜时,若阴极得到的电子数为2NA,则阳极质量减少64g | |
| D. | 3.2g由氧气和臭氧组成的混合物中含有氧原子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动,逆反应速率减小 | |
| B. | 平衡常数K增大 | |
| C. | NO2的转化率变大 | |
| D. | 容器内气体颜色先变深后变浅,最后比原来还要浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 | |
| D. | 金属腐蚀的电化学腐蚀,是利用了原电池原理,但原电池原理不能用于金属防护 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
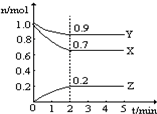 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.据此回答:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.据此回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com