
【题目】下列反应中,说明氨有还原性和碱性的是( )
A.2NH3+3CuO ![]() 3Cu+N2↑+3H2O
3Cu+N2↑+3H2O
B.8NH3+3Cl2═6NH4Cl+N2
C.4NH3+6NO ![]() 5N2+6H2O
5N2+6H2O
D.NH3+HCl═NH4Cl
【答案】B
【解析】解:A.在反应2NH3+3CuO ![]() 3Cu+N2↑+3H2O中,氮元素化合价升高,表现氨气的还原性,无铵盐生成,不能体现氨气的碱性,故A错误; B.在反应8NH3+3Cl2═6NH4Cl+N2 , 氮元素化合价升高,表现氨气的还原性,有铵盐生成,说明氨有还原性和碱性,故B正确;
3Cu+N2↑+3H2O中,氮元素化合价升高,表现氨气的还原性,无铵盐生成,不能体现氨气的碱性,故A错误; B.在反应8NH3+3Cl2═6NH4Cl+N2 , 氮元素化合价升高,表现氨气的还原性,有铵盐生成,说明氨有还原性和碱性,故B正确;
C.在反应4NH3+6NO ![]() 5N2+6H2O中,氮元素化合价升高,表现氨气的还原性,无铵盐生成,不能体现氨气的碱性,故C错误;
5N2+6H2O中,氮元素化合价升高,表现氨气的还原性,无铵盐生成,不能体现氨气的碱性,故C错误;
D.在反应NH3+HCl═NH4Cl中氮元素化合价不变,生成铵盐,只体现氨气的碱性,故D错误;
故选:B.
【考点精析】本题主要考查了氨的化学性质的相关知识点,需要掌握与水反应,NH3是惟一能使润湿的红色石蕊试纸交蓝的气体,常用此性质检验NH3;与酸反应:NH3+HCl=NH4Cl(生成白烟);与O2反应:4NH3+5O2=4NO+6H2O+Q;


 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是( )
酸 | 碱 | 盐 | 氧化物 | |
A | 硫酸 | 纯碱 | 石膏 | 铁红 |
B | 氢硫酸 | 烧碱 | 纯碱 | 生石灰 |
C | 碳酸 | 熟石膏 | 小苏打 | 二氧化硫 |
D | 二氧化碳 | 苛性钾 | 食盐 | 石灰石 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.08mol/L.
(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入碘化氢0.4mol,求达到平衡时碘化氢的转化率和氢气的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(氧氮杂 ![]() 是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质.下面是某研究小组提出的一种氧氮杂
是新药研制过程中发现的一类重要活性物质,具有抗惊厥、抗肿瘤、改善脑缺血等性质.下面是某研究小组提出的一种氧氮杂 ![]() 类化合物H的合成路线:
类化合物H的合成路线: 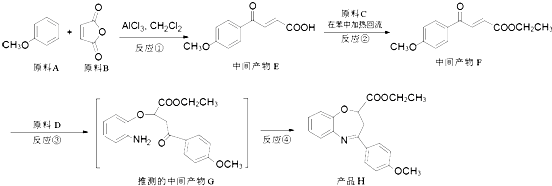
(1)原料A的同分异构体中,含有苯环、且核磁共振氢谱中有4个峰的是(写出其结构简式).
(2)反应②的化学方程式是 .
(3)③的反应类型是 . 原料D中含有的官能团名称是、 .
(4)原料B俗名“马莱酐”,它是马莱酸(顺丁烯二酸: ![]() )的酸酐,它可以经下列变化分别得到苹果酸(
)的酸酐,它可以经下列变化分别得到苹果酸( ![]() )和聚合物Q:
)和聚合物Q: 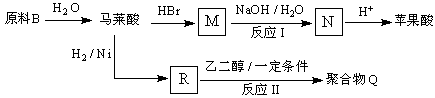
写出反应Ⅰ和反应Ⅱ的化学方程式:、 .
(5)符合下列条件的中间产物F的同分异构体数目是(不考虑手性异构),写出其中任意一种的结构简式 . (i)能发生银镜反应;
(ii)分子中含有三取代的苯环结构,其中两个取代基是:﹣COOCH3和 ![]() ,且二者处于对位.
,且二者处于对位.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子的立体构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH3═CH2 ③苯 ④CH≡CH ⑤NH3 ⑥CH4 ⑦HCHO.
A.①②③⑦
B.①⑤⑥
C.②③④⑦
D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列两套装置的描述不正确的是( ) 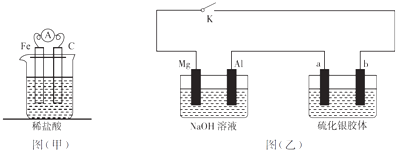
A.甲装置为铁的析氢腐蚀,若将铁换成铜,则甲装置就是铜的吸氧腐蚀
B.若将甲装置中的电流表改为电源,无论电源怎么连接,C电极上都会有气体放出
C.乙装置中K关闭后,a极附近颜色逐渐加深变黑
D.若将乙装置中的NaOH溶液换为HCl溶液,则K关闭后b极颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出).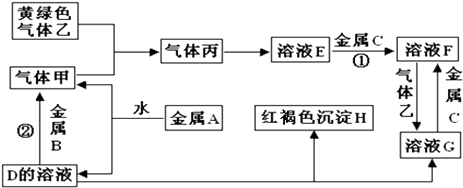
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A;H; G;乙;
(2)写出下列反应的化学方程式反应①反应② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是( ) 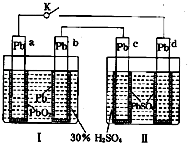
A.K闭合时,d电极反应式:PbSO4+2H2O﹣2e﹣=PbO2+4H++SO42﹣
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol
C.K闭合时,II中SO42﹣向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验Ⅰ:下图1为实验室制取氨的实验装置。

(1)写出A中所发生反应的化学方程式____________________________________。
(2)在收集氨时试管口棉花的作用是______________________________________。
(3)另一学生积极思考产生喷泉的其他方法,设计了图3装置。首先在锥形瓶中分别加入足量的下列物质,反应后产生喷泉的是(____)
A.CaCO3粉末和浓盐酸 B.NH4HCO3溶液与稀NaOH溶液
C.HCl和AgNO3溶液 D.HCl和酚酞溶液
(4)该同学又向锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是(____)
A.硝酸铵 B.食盐 C.浓硫酸
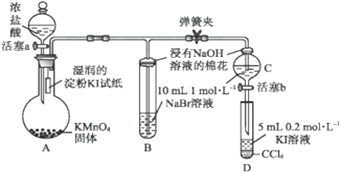
实验Ⅱ:为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为橙黄色时,夹紧弹簧夹。
Ⅲ.当B中橙黄色溶液颜色变深时,关闭活塞a。
Ⅳ. 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。
(1)A中产生黄绿色气体,其化学方程式是__________________
(2)B中溶液发生反应的离子方程式是____________________
(3)过程Ⅳ的目的为______________________________________
(4)D中出现的现象为____________________________
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下_________,得电子能力逐渐减弱。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com