
下列说法正确的是
A.HNO3的摩尔质量为63
B.摩尔是物质的量的单位
C.1 mol任何物质都约含有6.02×1023个原子
D.64 g SO2中含有1mol O2
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:2014-2015学年甘肃省高三11月月考化学试卷(解析版) 题型:实验题
(19分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
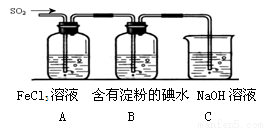
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 。
(2)装置C的作用是 。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯
E.玻璃棒
F.坩埚
(4)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成 ;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42—。该做法 (填“合理”或“不合理”),理由是 。
(5)能表明I-的还原性弱于SO2的现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
水的状态除了气、液、固之外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固态形状,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.玻璃态水是一种特殊的分子晶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
某工厂排出的废液中含有Ba2+、Ag+、Cu2+,用①Na2CO3溶液,②NaOH溶液,
③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是
A.②③① B.③②① C.①②③ D.③①②
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
下列实验操作正确的是
A.过滤时为加快速度,可先将上层清液注入过滤器中,再将沉淀转移到过滤器中
B.蒸发时用玻璃棒搅拌,是为了使析出的固体重新溶解
C.蒸馏时需从冷凝管上口进水,下口出水
D.分液时,下层液体放完后,再从下口放出上层液体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:实验题
(12分)用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-(aq)+5H2C2O4(aq)+6H+(aq)=2Mn2+(aq)+10CO2(g)+8H2O(l) ΔH<0
一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化,所用注射器的容积充裕):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
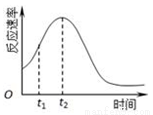
(1)该实验探究的是 因素对化学反应速率的影响,如果实验完成时草酸与KMnO4均有剩余,则相同时间内针筒中所得CO2体积大小关系是: < (填实验序号)研究发现反应速率总是如图所示发生变化,则t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂,② 。
(3)若实验①在4 min末收集了4.48 mL CO2(标准状况),则4 min末c(MnO4-)= mol·L-1(假设溶液混合后体积为50 mL),此4 min内的平均速率为v(H2C2O4)= 。
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可以通过测定 来比较化学反应速率。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
碘与氢气反应的热化学方程式为:
①I2(g)+H2(g)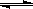 2HI(g) ΔH= - 9.48 kJ·mol-1
2HI(g) ΔH= - 9.48 kJ·mol-1
②I2(s)+H2(g)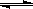 2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
A.反应①的产物比反应②的产物稳定
B.I2(s)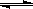 I2(g) ΔH= + 17.00 kJ·mol-1
I2(g) ΔH= + 17.00 kJ·mol-1
C.反应②的反应物总能量比反应①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市宝坻区四校高一11月联考化学试卷(解析版) 题型:填空题
X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):
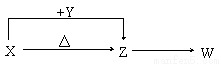
请回答:
⑴W的化学式是____________________。
⑵X与Y在溶液中反应的离子方程式是_______________________________。
⑶①将4.48 L(已折算为标准状况)W通入100 mL3 mol/L的Y的水溶液后,溶液中的溶质是________。
②自然界中存在X、Z和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100 mL溶液,测
得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为 g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市宝坻区四校高二11月联考化学试卷(解析版) 题型:选择题
关于强、弱电解质的叙述正确的是
A.强电解质都是离子化合物,弱电解质都是共价化合物
B.强电解质都是可溶性化合物,强电解质都是难溶性化合物
C.强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子
D.强电解质的水溶液导电能力强,弱电解质的水溶液导电能力弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com