
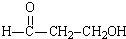 加入到足量的酸性KMnO4溶液中,充分反应后生成丙二酸,锰元素在生成物中为+2价,则消耗KMnO4的物质的量是( )
加入到足量的酸性KMnO4溶液中,充分反应后生成丙二酸,锰元素在生成物中为+2价,则消耗KMnO4的物质的量是( )| A. | 0.4mol | B. | 0.6mol | C. | 0.8mol | D. | 1.2mol |
分析 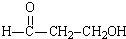 转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,根据电子守恒计算.
转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,根据电子守恒计算.
解答 解: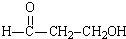 转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,
转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,
设消耗的KMnO4的物质的量为nmol,
则1mol×($\frac{4}{3}$+$\frac{2}{3}$)×3=5×n,
解得n=1.2mol.
故选D.
点评 本题考查了氧化还原反应的计算,注意根据电子守恒计算,题目难度不大,注意根据在化合物中正负化合价代数和为零计算有机物中C元素的化合价.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 所含质子数为(A-n) | B. | 所含中子数为(A-Z) | ||
| C. | 所含电子数为(Z+n) | D. | 中子数-电子数=A-2Z-n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
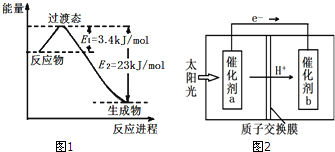 空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.| 温度(℃) | 300 | 500 | 700 |
| K | 3.00 | 3.47 | 4.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 用锌和足量稀硫酸制取氢气时加入硫酸铜溶液 | 可以加快制取氢气的速度 | Ⅰ对、Ⅱ对、无 |
| B | 用Mg-Al-NaOH构成原电池 | Mg更活泼作负极 | Ⅰ对、Ⅱ对、无 |
| C | 石墨常用做电解池的电极 | 石墨的化学性质稳定且导电性好 | Ⅰ对、Ⅱ对、有 |
| D | MgCl2是离子化合物 | 电解MgCl2的饱和溶液制取金属镁 | Ⅰ对、Ⅱ对、有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
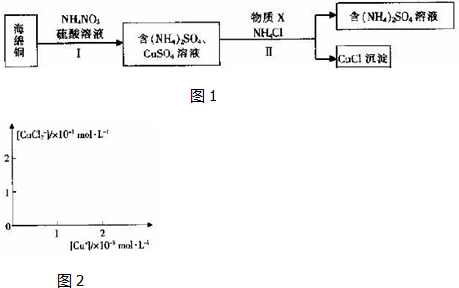
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g Na2O2中含有的阴离子数目为0.1NA | |
| B. | 常温下,34gH2O2中H-O键数目为2NA | |
| C. | 1.00mol NaCl晶体中含有NA个NaCl分子 | |
| D. | 在20g D216O中含有10 NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 只有①③④⑤ | C. | ②③④⑤ | D. | 只有①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com