
��15�֣�ijʵ��С������ͼ��ʾװ���Ʊ�һ�����ױ��������������ױ����������ױ�����
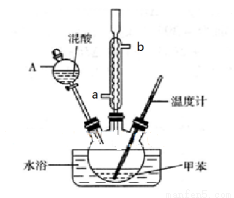
��Ӧԭ����
ʵ���п����õ������ݣ�
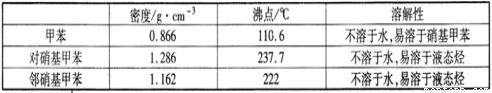
ʵ�鲽�裺��Ũ������Ũ���ᰴ�����1��3���ƻ����Һ�������ᣩ��40 mL��
��������ƿ�м���13g�ױ����ӷ�������ͼ��ʾװ��ҩƷ������������
��������ƿ�м�����
�ܿ����¶�ԼΪ50�棬��Ӧ��Լ10 min������ƿ���д�������ɫ��״Һ����֣�
�ݷ����һ�����ױ������ᴿ���յõ�������һ�����ױ���15 g��
��ش��������⣺
��1��ʵ��ǰ��Ҫ������ƿ�м�������________��Ŀ����____________________��
��2�������ܵ�������_________����ȴˮ�������ܵ�_______���a����b�����˽��롣
��3������A��������________ ��ʹ�ø�����ǰ������еIJ�����_________________��
��4�����뷴Ӧ�����ķ������£�

���У�����1������Ϊ________������2����IJ��������оƾ��ơ��¶ȼơ���ƿ��ţ�ǹܣ�β�ӹܣ���________________��_________________��
��5����ʵ����һ�����ױ��IJ���Ϊ________���������С�����һλ���֣���
��1����ʯ�������Ƭ����1�֣� ��ֹ���У�1�֣�
��2������������1�֣� a��1�֣�
��3����Һ©����1�֣� ����Ƿ�©Һ��1�֣�
��4����Һ��2�֣� ������ƿ��2�֣� �����ܣ�2�֣�
��5��77.5%��3�֣�
��������
�����������1������Һ�����������У�����ʵ��ǰ��Ҫ������ƿ�м���������ʯ�������Ƭ����Ŀ���Ƿ�ֹ���С�
��2����Ϊ��Ӧ��ױ���HNO3�ӷ������������ܵ���������ů������������ˮ������ʱ������Ч���ã�������ȴˮ�������ܵ�a�˽��롣
��3������װ��ͼ��֪������A�������Ƿ�Һ©����ʹ�÷�Һ©��ǰ������еIJ����ǣ�����Ƿ�©Һ��
��4������1�ѻ��Һ����Ϊ�л��������������������1Ϊ��Һ������2�ѻ��ܵ������л�����룬Ϊ������Ҫ��������������ƿ�������ܡ�
��5��13g�ױ������Ͽ����������ױ�Ϊ��13g��92g/mol��137g.mol=19.36g����һ�����ױ��IJ���Ϊ��15g��19.36g��100%=77.5%
���㣺���⿼�黯ѧʵ�����������������������ѧ���㡣


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014������5�¸����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ�У���ȷ����
A��NH4HCO3��Һ�����NaOH��Һ��Ӧ��NH4+ + OH- = NH3��H2O
B���ڱ��ӵ�������Һ�еμ�̼������Һ����壺2C6H5OH + CO32- �� CO2��+ 2C6H5O- + H2O
C��������ͭ�����缫������2H+ + 2Cl�� 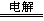 H2�� + Cl2��
H2�� + Cl2��
D��SO2ͨ�����������Һ�У�SO2 + ClO��+ H2O = SO42�� + Cl��+ 2H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������������������ѧ�ڵڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�����۵�Ĺ�������������Ӿ��壬��һ��Ϊԭ�Ӿ���
B�������������ǿ������������ԣ�����֪�����ԣ�Cl2>S
C��������Ԫ����ɵĹ��ۻ���������У�ֻ���ܴ��ڼ��Լ�
D����X+ ��Y2���ĺ�����Ӳ�ṹ��ͬ����ԭ��������X>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������������ǰģ�����ۻ�ѧ��ѧ�Ծ��������棩 ���ͣ������
��13�֣�
�л���A������ת����ϵ����A������ͼ���ʺɱ����ֵΪ88���������C��H��O����Ԫ�ص�������Ϊ6��1��4����A����ʹBr2��CCl4��Һ��ɫ��1mol B��Ӧ������2mol C��
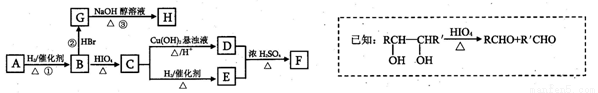
��ش��������⣺
��1��C��E�ķ�Ӧ����Ϊ ��
��2�����٣��ڡ���������Ӧ�IJ��ʷֱ�Ϊ93��0%��81��0%��88��0%������A�ϳ�H'���ܲ���Ϊ ��
��3��A�Ľṹ��ʽΪ ��
��4��д��C��������Һ��Ӧ�����ӷ���ʽΪ____��
��5��H����������̼ԭ�Ӿ���һ��ֱ���ϣ�Gת��ΪH�Ļ�ѧ����ʽΪ ��
��6��X��A��һ��ͬ���칹�壬����˴Ź���������3���壬�����֮��Ϊ1��1��2��1mol X����HIO4���ȵ������·�Ӧ������ֻ��1mol Y����X�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������������ǰģ�����ۻ�ѧ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A��lmol Cl2ͨ�뺬��2mol FeI2����Һ�У�2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B������ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+ HCO3-=CaCO3��+H2O
C��AlCl3��Һ�м��������ˮ��Al3++4 OH-= AlO-2+2H2O
D����������Һ�м������������[Ag(NH3)2]++OH-+3H+= Ag++2NH4++ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʱȽ��в���ȷ����
A���е�ĸߵͣ�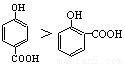 B���۵㣺SiO2>CsCl>CBr4>CF4
B���۵㣺SiO2>CsCl>CBr4>CF4
C��Ӳ�ȣ�þ>��>þ���Ͻ� D. ˮ���ԣ�HF>Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��11 �֣���ԭ������Դ����������ͷ�չ����Ҫ֧�����о���ѧ��Ӧ�����е������仯����Դ��ȱ�Ľ��������Ҫ���������壬��֪�����Ȼ�ѧ����ʽ
�� | H2��g��+ | |||||||||
�� | 2H2��g��+ O2��g��= 2H2O��l�� ��H =��572kJ/mol�� | |||||||||
�� | C��s��+ | |||||||||
�� | C��s��+ O2��g��= CO2��g�� ��H =��393.5kJ/moL�� | |||||||||
�� | CO2��g��+ 2H2O��g��= CH4��g��+ 2O2��g����H = + 802kJ/moL | |||||||||
��ѧ�� | O=O | C-C | H-H | O-O | C-O | O-H | C-H | |||
����kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 | |||
�ش���������
��1��д���ܱ�ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ ��
��2����֪C��s��+ H2O��g�� H2��g��+ CO��g����H = ___________ kJ/moL��
H2��g��+ CO��g����H = ___________ kJ/moL��
��3�������C=O����Ϊ kJ/moL��
��4��CH4��ȼ���ȡ�H = �� ___________ kJ/moL��
��5��25�桢101kPa�£�ijȼ����CH4��ȼ��Ч����90%��ע���൱��10%��CH4δȼ�գ���ˮ����������������70%�����ô�ȼ�ߺ�ˮ�����տ�1Lˮ����Ҫ��CH4�����ʵ���Ϊ_________mol[������С�����2λ����֪��c (H2O)=4.2 J/(g����) ]��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
(ԭ��) ���л�ѧ����ʹ����ȷ����
A��N2�Ľṹʽ��N = N
B��H2O�ı���ģ�ͣ�
C��HClO�ĵ���ʽ��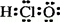
D��MgBr2���γɹ����õ���ʽ��ʾΪ��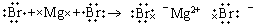
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����������������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���ڼ��ȡ���ȩ������(NH4)2SO4��Һ��X���������£������ʶ��ᷢ������
B�������ᡢ�����ʡ���֬������C��H��O��N����Ԫ��
C��������ʳ�õ�ʳ�ס�ֲ���͡����ﵰ�����ʶ��ǻ����
D����ϩ������ϩ���ױ�����ʹ���Ը��������Һ��ɫ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com