
将金属铜、铁置于氯化铁溶液中充分反应,下列对反应情况设想的评价正确的是 ( )
选项 | 反应情况设想 | 评价 |
A | 当铁、铜均不剩余时,溶液中一定有Fe2+、Cu2+,一定无Fe3+ | 正确,Fe3+和Fe、Cu均可反应 |
B | 当铁、铜均有剩余时,溶液中一定有Fe2+、Cu2+、无Fe3+ | 正确,Fe和Cu与Fe3+都反应,故有Fe2+和Cu2+,无Fe3+ |
C | 当铜有剩余,铁无剩余时,溶液中一定只有Fe2+,无Cu2+ | 正确,Cu有剩余,故无Cu2+ |
D | 当铁有剩余,铜无剩余时,溶液中一定有Fe2+、Cu2+ | 不正确,不可能有Fe剩余而无Cu剩余,因为Fe比Cu优先与Fe3+反应 |
D
【解析】
试题分析:A、当铁铜均不剩余时,Fe3+和Fe、Cu均可反应,故溶液中一定有Fe2+、Cu2+,若恰好完全反应,则无Fe3+,若氯化铁过量,则含有Fe3+,故A错误;B、当铁铜均有剩余时,Fe与Cu2+和Fe3+都反应,故溶液中一定有Fe2+,无Fe3+、Cu2+,故B错误;C、当铜有剩余,铁无剩余时,溶液中一定有Fe2+,若铁与Cu2+恰好完全反应,则无Cu2+,若Cu2+过量,则含有Cu2+,故C错误;D、不可能有Fe剩余,Cu不剩余,因为Fe比Cu优先与Fe3+反应,故D正确;故选:D。
考点:考查Fe与Cu的金属性强弱以及Fe与Cu与氯化铁反应后溶液中所含离子的判断


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:填空题
(18分)某校化学实验兴趣小组在“探究卤索单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
提出问题 Fe3+、Br2谁的氧化性更强?
(1 )猜 想: ①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(2)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 |
方案1 |
|
|
方案2 |
|
|
(3)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入l~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(4)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是:
(填离子的化学式)。
②在100 mL FeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
2014年9月28日,郑州市区被大雾笼罩,空气严重污染,其首要污染物为PM2.5。PM2.5是指大气中直径小于或等于2.5×10-6m的颗粒物,又称可入肺颗粒物。下列有关说法不正确的是
A.雾是由大量悬浮在近地面空气中的微小水滴或冰晶组成的气溶胶,多出现于秋冬季节
B.焚烧秸秆和化石燃料的燃烧会增大空气中PM2.5的含量
C.PM2.5在空气中一定能产生丁达尔现象
D.开发利用新能源,实施“低碳经济”,可减少PM2.5的产生
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列现象或事实不能用同一原理解释的是
A.浓硝酸和氯水用棕色细口试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.Cl2和SO2都能使品红溶液褪色
D.SO2和FeSO4溶液都能使KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.化石燃料燃烧产生大量CO2,会导致温室效应
B.血液透析利用了胶体的性质
C.自来水可用氯气来杀菌消毒,说明氯气无毒
D.采用原煤脱硫技术,可减少燃煤燃时产生的SO2
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
下列有关说法正确的是 ( )
A.1 mol Cl2参加反应转移电子数一定为2NA
B.反应Li2NH+H2 LiNH2+LiH中H2既是氧化剂又是还原剂
LiNH2+LiH中H2既是氧化剂又是还原剂
C.在反应KIO3+6HI===KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA
D.根据反应中HNO3(稀)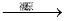 NO,而浓硝酸
NO,而浓硝酸 NO2可知,氧化性HNO3(稀)>浓硝酸
NO2可知,氧化性HNO3(稀)>浓硝酸
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
下列有关说法中正确的是 ( )
A.有单质生成的反应一定是氧化还原反应
B.焰色反应是元素表现出来的化学性质
C.由两种元素组成,原子个数比为1:1的物质一定是纯净物
D.能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:填空题
(12分)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理,常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
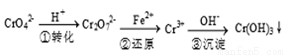
其中第①步存在下列平衡:2CrO42- (黄色) +2H+  Cr2O72-(橙色) +H2O
Cr2O72-(橙色) +H2O
(1)若平衡体系的pH=2,该溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
A.Cr2O72-和CrO42-的浓度相同
B.2V(Cr2O72-)=V(CrO42-)
C.溶液的颜色不变
(3)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡
Cr(OH)3(s)  Cr3+(aq)+3OH-(aq) Ksp Cr(OH)3=c (Cr3+)?c3(OH-)=10-32
Cr3+(aq)+3OH-(aq) Ksp Cr(OH)3=c (Cr3+)?c3(OH-)=10-32
常温下,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至__________。
方法2电解法:
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(4)用Fe做电极的原因为 。
(5)在阴极附近溶液pH升高的原因(用电极反应式解释) ,溶液中同时生成的沉淀还有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列关于试剂存放的叙述正确的是
A.硝酸银溶液存放在无色试剂瓶中
B.金属钠保存在CCl4中(钠的密度小于CCl4)
C.浓硫酸的装运包装箱应贴上如图所示的标识
D.氢氧化钠溶液保存在带玻璃塞的玻璃瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com