
【题目】下列有关同分异构体数目的叙述中,正确的是
A.不考虑空间异构,C2H6O的一氯代物有3种结构
B.分子式符合C5H11Cl的化合物有6种
C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目多于3种
D.菲的结构简式为![]() ,它与硝酸反应可生成6种一硝基取代物
,它与硝酸反应可生成6种一硝基取代物
【答案】A
【解析】
A.不考虑空间异构,C2H6O有乙醇和二甲醚2种,乙醇的一氯代物有2种,二甲醚的一氯代物有1种结构,共3种,故A正确;
B.分子式为C5H11Cl的同分异构体有:主链有5个碳原子的:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;主链有4个碳原子的:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;主链有3个碳原子的:CH2C(CH3)2CH2Cl,所以共有8种情况,故B错误;
C.由于苯环含有6个H原子,二氯苯与四氯苯的同分异构体数目相同,若二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种,故C错误;
D.菲的结构简式为![]() ,为对称结构,有如图所示的5种H原子
,为对称结构,有如图所示的5种H原子 ,所以与硝酸反应,可生成5种一硝基取代物,故D错误;
,所以与硝酸反应,可生成5种一硝基取代物,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】(一)实验室用图甲装置制备SO3并测定SO2催化氧化为SO3的转化率。
已知:SO3熔点为16.8℃,沸点为44.8℃,假设气体进入装置可以被完全吸收,不考虑空气的影响。

(1)A中使用浓硫酸的质量分数为70%的原因是___,B中浓H2SO4的作用是___。
(2)当实验停止通入SO2,熄灭酒精灯后,还需要继续通一段时间的氧气,其目的是___。
(3)实验结束后测得装置D增加了ag,装置E中的沉淀洗涤烘干后其质量为bg。则E中的沉淀的化学成分是___(填写化学式),本实验中SO2转化率为___(用代数式表示,不用化简)。
(二)SO3溶于浓硫酸后可得到发烟硫酸,工业上把干燥的氯化氢气体通入到发烟硫酸中可以得到HSO3Cl。HSO3Cl是一种无色液体,沸点为152℃,有强腐蚀性,遇湿空气产生强烈的白雾。现用图乙所示的装置制取HSO3Cl(夹持及加热装置略去)。

(1)HSO3Cl遇湿空气产生强烈的白雾,请结合用化学方程式解释其原因___。
(2)分液漏斗下方接的毛细管,其作用是___;若不用毛细管而直接用分液漏斗注入浓盐酸,可能发生的现象是___。
(3)装置F的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有__________。
(2)磷精矿粉酸浸时发生反应:
2Ca5(PO4)3(OH)+3H2O+10H2SO4![]() 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
①该反应体现出酸性关系:H3PO4__________H2SO4(填“>”或“<”)。
②结合元素周期律解释①中结论:P和S电子层数相同,__________。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:__________。
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:____________________。

(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42残留,原因是__________;加入BaCO3可进一步提高硫的脱除率,其离子方程式是____________________。
(6)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用b mol·L1NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液c mL,精制磷酸中H3PO4的质量分数是________。(已知:H3PO4摩尔质量为98 g·mol1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,在500℃时发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是
CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是

A.从反应开始到10min时,H2的平均反应速率v(H2)=0.15 mol/(L·min)
B.从20min到25min达到新的平衡,可能是增大压强
C.其他条件不变,将温度升到700℃,再次达平衡时平衡常数减小
D.从开始到25min,CO2的转化率是70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________。
(2)丙溶液中存在的电离平衡为______________(用电离平衡方程式表示)。
(3)常温下,用水稀释0.1 mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是________(填序号)。
①n(H+) ②c(H+) ③ c(CH3COOH)/c(CH3COO-) ④c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为___________。
(5)某同学用甲溶液分别滴定20.00 mL乙溶液和20.00 mL丙溶液,得到如图所示的两条滴定曲线,请回答有关问题:
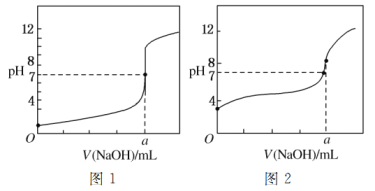
①甲溶液滴定丙溶液的曲线是________(填“图1”或“图2”)曲线。
②a=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是生物体内四种有机物的组成与功能关系图,有关叙述不正确的是 ( )
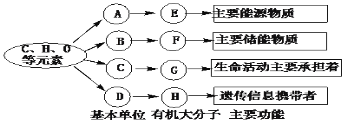
A. 玉米种子细胞中,物质A和E分别代表葡萄糖和纤维素
B. 相同质量的E和F彻底氧化分解,释放能量较多的是F
C. 在人体细胞中物质C约有20种
D. 不同的H在结构上的区别主要是碱基的排列顺序不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水产养殖户常用电解法净化鱼池中的水,其工作原理如下图所示。下列说法中正确的是

A. X极是电源的负极,发生氧化反应
B. 工作过程中阴极区溶液的pH逐渐减小
C. 当电路中转移10mole-时,Ⅱ极上产生22.4LN2
D. I极上的电极反应式:C6H12O6-24e-+6H2O==6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列叙述正确的是( )
为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,![]() 三氯甲烷中含有氯原子的数目为
三氯甲烷中含有氯原子的数目为![]()
B.![]() 葡萄糖中含羟基数目为
葡萄糖中含羟基数目为![]()
C.常温下,![]() 醋酸铵溶液(
醋酸铵溶液(![]() )中
)中![]() 与
与![]() 数目均为
数目均为![]()
D.![]() 和
和![]() 组成的混合物中含有的离子总数为
组成的混合物中含有的离子总数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com