
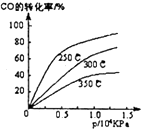
 ��ҵ�ϳɼ״���Ӧ���£�CO��g��+2H2��g��?CH3OH��g������H��ش��������⣺
��ҵ�ϳɼ״���Ӧ���£�CO��g��+2H2��g��?CH3OH��g������H��ش��������⣺���� ��1���ٴӺ�������һ�㣬��һ��ƽ��������������ߣ�����ͬѹǿ�²�ͬ�¶�ʱCO��ƽ��ת���ʣ��¶�Խ��ת����Խ�ͣ�˵��������ʱƽ���������ƶ���
�ڸ��ݷ�Ӧǰ���������ʵ����ı仯�жϡ�S�����ݡ�G=��H-T��S�жϷ�Ӧ�Է������⣬��Ӧ�ʱ��H-T��S��0��Ӧ�Է����У�
��2������������ʽ����ƽ��ʱ����ֵ�ƽ��Ũ�ȣ��ٸ��ݻ�ѧƽ�ⳣ������ʽ���㣻
������ѹǿ�������淴Ӧ���ʶ�����ƽ��������Ӧ����ƽ��ʱ����ֵ�Ũ�ȶ����ݴ��жϣ�
�۸������ԭƽ����ͬ˵��Ϊ��Чƽ�⣬���º��ݣ�ǰ����������仯������ѧ������ת������ߣ�����������ʵ����ʵ�����ȼ��ɣ��ݴ˽��a��b�Ĺ�ϵ��
�����ƽ��ʱCH3OH��g�������ʵ�����c���ڴ�ֵƽ�����淴Ӧ���У�����ѧ������ת������ߣ��õ�3mol COʱc��ֵ��ݴ˼�����
��� �⣺��1���ٴӺ�������һ��0.5������һ��ƽ��������������ߣ�����ͬѹǿ�²�ͬ�¶�ʱCO��ƽ��ת���ʣ��¶�Խ��ת����Խ�ͣ�˵��������ʱƽ���������ƶ����淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ��H��0��
�ʴ�Ϊ������
��CO��g��+2H2��g��?CH3OH��g������H��0���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����ؼ�С������S��0��
�ɡ�G=��H-T��S��0����Ӧ�Է����У���֪�÷�Ӧ�ڵ��������Է����У������²����Է����У��÷�Ӧ��һ���Է����У�
�ʴ�Ϊ����һ����
��2����3molCO��6molH2����2L���ܱ������У�CO��H2����ʼŨ�ȷֱ�Ϊ��$\frac{3mol}{2L}$=1.5mol/L��$\frac{6mol}{2L}$=3mol/L����ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.5 mol/L��COŨ�ȱ仯Ϊ1.5mol/L-0.5mol/L=1mol/L����
CO��g��+2H2��g��?CH30H��g��
��ʼ��mol/L����1.5 3 0
�仯��mol/L����1 2 1
ƽ�⣨mol/L����0.5 1 1
�ʸ��¶��£��÷�Ӧ��ƽ�ⳣ��K=$\frac{1}{{1}^{3}��0.5}$=2��
�ʴ�Ϊ��2��
��a������ѹǿ��ƽ��ʱ������Ũ������a����
b������ѹǿ����Ӧ��������Ũ�ȶ����������淴Ӧ���ʶ��ӿ죬��b��ȷ��
c������ѹǿƽ��������Ӧ�����ƶ���һ����̼��ת�������ӣ���c��ȷ��
�ʴ�Ϊ��a��
�۸������ԭƽ����ͬ˵��Ϊ��Чƽ�⣬���º��ݣ�ǰ����������仯������ѧ������ת������ߣ�����������ʵ����ʵ�����ȼ��ɣ������У�a+c=3��b+2c=6��������b=2a��
�ɢټ����֪��ƽ��ʱCH3OH�����ʵ���Ϊ1mol/L��2L=2mol������c��2molƽ�����淴Ӧ���У�����ѧ������ת������ߣ��õ�3mol COʱc��ֵ�������c���Ϊ3mol������2��c����3��
�ʴ�Ϊ��b=2a��2��c��3��
���� �����ۺ��Խϴ��漰��ѧ��Ӧ�Է����жϡ���ѧƽ�ⳣ������ѧƽ��Ӱ�����ء���Чƽ������֪ʶ����Ŀ�Ѷ��еȣ���2����ע���Ч˼��������Լ����ü�����ȷ��c��ȡֵ��Χ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HF�����ȶ��Ժܺã�����ΪHF���Ӽ������� | |
| B�� | ���ɵ��ʷ��ӵ�����֮�䲻һ�����ڹ��ۼ� | |
| C�� | �ɷǽ���Ԫ����ɵĻ����ﲻһ���ǹ��ۻ����� | |
| D�� | ���������Ӽ�ͨ�����Ӽ�һ�����γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɱ������� | B�� | �����������ʯ�ҵ��ۻ� | ||
| C�� | �Ȼ��ƺ������ۻ� | D�� | �Ҵ������������������ۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ZΪ0.4mol•L-1 | B�� | X2Ϊ0.2 mol•L-1 | C�� | Y2Ϊ0.4 mol•L-1 | D�� | ZΪ0.3 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢ� | C�� | �٢� | D�� | �ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �� ���Ӿ۷�Ӧ��
�� ���Ӿ۷�Ӧ�� �� ��ȡ����Ӧ��
�� ��ȡ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 28g��ϩ�������õ��Ӷ���ĿΪ4NA | |
| B�� | 1mol CH3+�����ĵ�������Ϊ10NA | |
| C�� | 0.5 mol�������к���C=C˫����Ϊ1.5 NA | |
| D�� | ��״���£�11.2 L��CH4��C2H4��ɵĻ�������к�����ԭ�ӵ���ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.0Ħ�� | B�� | 1.6Ħ�� | C�� | 2.2Ħ�� | D�� | 2.0Ħ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com