
化学与生活、科技关系密切。下列说法正确的是
A. 液氨可用作制冷剂是因为其气化时可放出大量的热
B. 将青蒿在乙醚中浸取,通过分馏可提取治疗疟疾的青蒿素
C. 钢制品、铝制品在日常生活中被广泛应用是因为铁、铝为活泼金属
D. 久置的漂白粉变质是因为漂白粉与空气中的O2反应
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
向Cr2(SO4)3的水溶液中加入Na0H溶液,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的亚铬酸根离子(CrO2-),其平衡关系为:
向50mL0.05mol/L的Cr2(SO4)3溶液中,加入l.0mol/L的NaOH溶液50mL,充分反应后,溶液中可观察到的现象为
A. 溶液为紫色 B. 溶液中有灰绿色沉淀 C. 溶液为亮绿色 D. 无法判断
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二3月学业水平测试化学试卷(解析版) 题型:选择题
下列叙述错误的是
A. 可用铝制容器盛装稀硫酸
B. Na2O2可用于呼吸面具中作为氧气的来源
C. Fe2O3常用于制造红色油漆和涂料
D. Si可用于制造太阳能电池
查看答案和解析>>
科目:高中化学 来源:2017届四川省乐山市高三第二次调查研究考试理科综合化学试卷(解析版) 题型:选择题
化学与人类生产、生活环境密切相关。下列说法正确的是
A. 化石燃料的大量开发和使用是导致温室效应和形成胶时酸雨的重要原因
B. 为消除碘缺乏病,政府规定在食盐中必须举加一定量的KI
C. 为了确保食品安全,应禁止使用食品添加剂
D. 为了提高农作物产量,应该大量使用农药和化肥
查看答案和解析>>
科目:高中化学 来源:2017届河南省安阳市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
硫酸锶(SrSO4)可用于烟火和陶瓷工业,该物质是矿物天青石的主要成分,可有Na2SO4溶液加入锶盐溶液沉淀而得。如图是硫酸锶的溶解曲线,下列说法正确的是
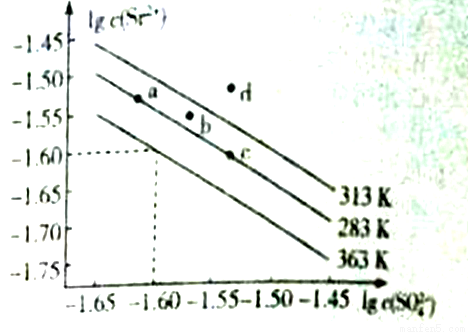
A. 图像中a、c两点的溶度积:Ksp(a)<Ksp(c)
B. 363K时的溶度积Ksp(SrSO4)=1.0×10-3.20
C. SrSO4的溶解度随温度升高而增大
D. 313K时,b点为饱和溶液,d点为不饱和溶液
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期第四次月考理科综合化学试卷(解析版) 题型:推断题
用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答:
(1)A元素是________,B元素是___________,C元素是__________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其结构式是__________________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是________________。
(4)F是由两种元素组成的三原子分子______,其电子式是________________。
(5)G分子中含有4个原子,它易溶于水的原因是________________
(6)A+与C2-形成的化合物水溶液呈_____性,其原因是(用离子方程式表示)___________,该水溶液中离子浓度由大到小的顺序是_____________。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上学期第四次月考理科综合化学试卷(解析版) 题型:选择题
化学与人类生产、生活、社会可持续发展密切相关。下列有关说法正确的是
A. 某地燃烧化石燃料排放的废气中含CO2、SO2,使雨水pH=6形成酸雨
B. 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
C. 高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2=2O3有单质参加,属于氧化还原反应
D. 人造纤维,合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市长望浏宁四县高三3月模拟考试理综化学试卷(解析版) 题型:简答题
从宏观现象探究微观本质是重要的化学学科素养。以FeCl3溶液为实验研究对象,探究其与碱性物质之间的复杂多样性。实验如下:
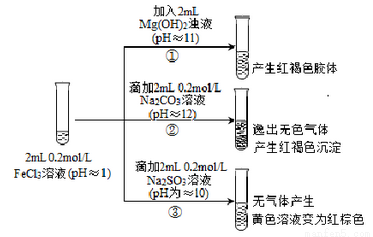
(1)①中反应的离子方程式是_________________。
(2)②中逸出的无色气体是_______________。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
Ⅰ.甲取③中的红棕色溶液少许,滴入少量盐酸酸化的BaCl2溶液,产生白色沉淀。 甲得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是______________。
Ⅱ.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是取Ⅰ中所得溶液少许进行__________离子的检验。
(4)受以上实验的启发,同学们对pH≈8的1mol/LNaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
实验操作及现象 | ④向2mL0.2mol/L FeCl3溶液中滴入2mL1mol/LNaF溶液。溶液变无色 |
⑤向2mL0.2mol/L FeCl3溶液中滴入2mL蒸馏水,溶液颜色变浅 |
Ⅰ.⑤的实验目的是___________。
Ⅱ.为探究④中溶液变无色的原因,进行如下实验:
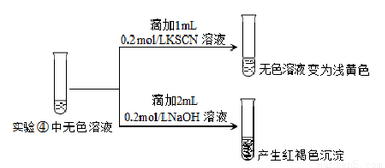
资料显示:FeF3溶液为无色。
用平衡移动原理解释红褐色沉淀产生的原因:_______________。
(5)根据实验,FeCl3溶液与碱性物质之间的反应的多样性与_____________________有关。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列事实不能用电化学原理解释的是
A. 可将地下输油钢管与外加直流电源的负极相连以保护钢管不受腐蚀
B. 常温条件下,铝在空气中不易被腐蚀
C. 镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更耐腐蚀
D. 用锌与稀硫酸刮氢气时,往稀硫酸中滴少量硫酸铜溶液能加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com