
【题目】I:在Na2SO3溶液中滴加酚酞,溶液变红色,若在该溶液中滴入过量的BaCl2溶液,现象是_________,请结合离子方程式,运用平衡原理进行解释_____________________。
II:等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,溶液显______性。此时溶液中浓度相等的微粒是___________________________________________。
III:已知:H2S:Ki1=1.3×10-7 Ki2=7.1×10-15 H2CO3:Ki1=4.3×10-7 Ki2=5.6×10-11,含H2S尾气用足量的Na2CO3溶液来吸收。写出离子反应方程式。____________,常温时,等体积等浓度的Na2S和Na2CO3溶液的离子总数:N前___N后(填“>”或“<”)。
【答案】有白色沉淀生成,溶液红色褪去 亚硫酸钠溶液水解呈碱性,滴入酚酞呈红色。SO32- +H2O![]() HSO3-+OH-,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去 中 H+与OH-、SO42-与Cl- H2S + CO32-→HS-+ HCO3- <
HSO3-+OH-,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去 中 H+与OH-、SO42-与Cl- H2S + CO32-→HS-+ HCO3- <
【解析】
Ⅰ.在Na2SO3溶液中滴加酚酞,溶液变红色,说明亚硫酸根离子水解,溶液显碱性,Na2SO3溶液与BaCl2溶液反应生成Ba2SO3沉淀,使SO32-水解平衡![]() 逆向移动,c(OH-)减小,所以酚酞褪色,本小题答案为:有白色沉淀生成,溶液红色褪去;亚硫酸钠溶液水解呈碱性,滴入酚酞呈红色。
逆向移动,c(OH-)减小,所以酚酞褪色,本小题答案为:有白色沉淀生成,溶液红色褪去;亚硫酸钠溶液水解呈碱性,滴入酚酞呈红色。![]() ,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去;
,加入氯化钡后,Ba2++SO32-→BaSO3↓,降低了SO32-的浓度,使得水解平衡往左移动,导致溶液中OH-浓度降低,因此溶液红色褪去;
Ⅱ.ClO-有氧化性,能够氧化SO32-,反应的离子方程式为![]() ,等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,生成相同浓度的NaCl和Na2SO4混合溶液,溶液显中性,H+与OH-、SO42-与Cl-离子浓度相等,本小题答案为:中;H+与OH-、SO42-与Cl-;
,等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,生成相同浓度的NaCl和Na2SO4混合溶液,溶液显中性,H+与OH-、SO42-与Cl-离子浓度相等,本小题答案为:中;H+与OH-、SO42-与Cl-;
Ⅲ.据弱酸的电离平衡常数可以知道其酸性![]() ,H2S与足量的Na2CO3溶液反应的离子方程式为: H2S
,H2S与足量的Na2CO3溶液反应的离子方程式为: H2S![]() ,HCO3-的酸性比HS-强,越弱越水解,所以Na2S溶液比Na2CO3溶液的碱性强,c(H+)小,据电荷守恒在碳酸钠溶液中有
,HCO3-的酸性比HS-强,越弱越水解,所以Na2S溶液比Na2CO3溶液的碱性强,c(H+)小,据电荷守恒在碳酸钠溶液中有![]() ,在硫化钠溶液中有
,在硫化钠溶液中有![]() ,等浓度的两溶液中,c(Na+)相同,所以硫化钠溶液中离子总浓度小于碳酸钠,等体积时, Na2S和Na2CO3溶液的离子总数: N前<N后,本小题答案为:<。
,等浓度的两溶液中,c(Na+)相同,所以硫化钠溶液中离子总浓度小于碳酸钠,等体积时, Na2S和Na2CO3溶液的离子总数: N前<N后,本小题答案为:<。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】M(NO3)2热分解化学方程式为2M(NO3)2![]() 2MO+4NO2↑+ O2↑,加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11.2 L的气体,那么M的摩尔质量是
2MO+4NO2↑+ O2↑,加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11.2 L的气体,那么M的摩尔质量是
A.24 g·mol-1B.74 g·mol-1
C.148 g·mol-1D.40 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物![]()
![]() 的说法正确的是
的说法正确的是
A. a、b互为同系物
B. c中所有碳原子可能处于同一平面
C. a、b、c均能使酸性高锰酸钾溶液褪色
D. b的同分异构体中含有羧基的结构还有7种(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃A可以从煤干馏得到的煤焦油中分离出来,以A为原料可以合成聚邻氨基苯甲酸、扁桃酸等物质,其合成流程如下(部分产物、合成路线、反应条件已略去):
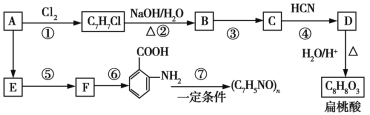
已知:
Ⅰ.R—CHO+HCN![]()
![]()
Ⅱ.R—CN![]() R—COOH
R—COOH
Ⅲ.![]()
![]()
![]() (苯胺易被氧化)
(苯胺易被氧化)
请回答下列问题:
(1)C的分子式为__________。
(2)下列对相关反应类型的判断合理的是__________ (填序号)。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
Ⅰ | 加成 | 水解 | 还原 | 取代 | 还原 | 氧化 | 加聚 |
Ⅱ | 加成 | 消去 | 还原 | 加成 | 氧化 | 还原 | 缩聚 |
Ⅲ | 取代 | 水解 | 加成 | 氧化 | 还原 | 缩聚 | |
Ⅳ | 取代 | 消去 | 氧化 | 取代 | 还原 | 氧化 | 加聚 |
(3)写出反应③的化学方程式:______________________________。
(4)扁桃酸有多种同分异构体,其中既能与氯化铁溶液发生显色反应,又能与碳酸氢钠溶液反应产生气泡的同分异构体有__________种,写出其中一种的结构简式:__________________。
(5)以芳香烃A为主要原料,还可以通过下列合成路线合成阿司匹林和冬青油:

①冬青油的结构简式为____________________。
②写出反应Ⅴ的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO![]() +5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
学习小组的同学设计了如下步骤用滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)上述步骤②中使用的锥形瓶是否需要事先用待测液润洗_______。(填“是”或“否”)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。

(2)本实验滴定达到终点的标志可以是________________________________。
(3)通过上述数据,求得x=________。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”、“偏小”或“不变”,下同)。
②根据上述实验计算的数据可信性不强,为了提高实验的准确性,请写出改进方法______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验目的 | 探究Na2CO3和NaHCO3溶解度的相对大小 | 用已知浓度的NaOH溶液滴定未知浓度的稀硫酸 | 检验蔗糖与浓硫酸反应产生的CO2 | 验证镁和稀盐酸的反应的热效应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中氟多以化合态形式存在,主要有萤石(CaF2)、冰晶石(Na3AlF6)等
(1)基态氟原子中,有_______种能量不同的电子。
(2)萤石(CaF2)难溶于水,但可溶于含Al3+的溶液中,原因是_________________(用离子方程式表示)。(已知AlF63-在溶液中可稳定存在)
(3)BF3与一定量的水形成(H2O)2BF3晶体Q,晶体Q在一定条件下可转化为R:

①晶体R中含有的化学键包括_________(填标号)。
A.离子键 B.配位键 C.共价键 D.氢键
②R中阳离子的空间构型为_________,阴离子中心原子的杂化方式为_________。
(4)F2与其他卤素单质反应可以形成卤素互化物,如ClF3、BrF3等。ClF3的熔沸点比BrF3的低,原因是___________________________________。
(5)Na3AlF6晶胞结构如图所示:

①位于大立方体体心▽代表________(填离子符号);
②AlF63-做面心立方最密堆积形成正四面体和正八面体两种空隙,正四面体空隙数和AlF63-数之比为_______,其中_________%正八面体空隙被Na+填充;
③晶胞边长为x nm,则相距最近的两个Na+之间距离为_____ nm;设Na3AlF6的相对分子质量为M,阿伏加德罗常数为NA,则该晶体密度的计算表达式为________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分))对于A+2B(气)![]() nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
(1)A量的增减,平衡不移动,则A为______态。
(2)增压,平衡不移动,当n=2时,A的状态为________;当n=3时,A的状态为______。
(3)若A为固体,增大压强,C的组分含量减少,则____。
(4)升温,平衡向右移动,则该反应的逆反应为________反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com