
【题目】固体化合物X由3种元素组成。某学习小组进行了如下实验:
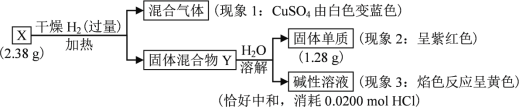
请回答:
(1) 由现象1得出化合物X含有________元素(填元素符号)。
(2) 固体混合物Y的成分________(填化学式)。
(3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的化学方程式是________。
【答案】O Cu和NaOH NaCuO2 2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O
【解析】
固体混合物Y溶于水,得到固体单质为紫红色,说明是Cu,产生碱性溶液,焰色反应呈黄色说明含有钠元素,与盐酸HCl中和,说明为NaOH(易算出为0.02mol),混合气体能使CuSO4变蓝,说明有水蒸汽。
(1)CuSO4由白色变为蓝色,说明有水生成,根据元素守恒分析,必定含有O元素。
(2)现象2获得紫色单质,说明Y含有Cu,现象3焰色反应为黄色说明有Na元素,与HCl发生中和反应说明有NaOH,故答案填Cu和NaOH。
(3)NaOH为0.02mol,易算出m(Na)=0.02×23g=0.46g,m(O)=m-m(Na)-m(Cu)=2.38-0.46-1.28=0.46g,N(Na):N(Cu):N(O)=![]() =1:1:2,故化学式为NaCuO2,X与浓盐酸反应,根据反应现象,产物有Cl2,和CuCl2蓝色溶液,因而化学方程式为2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O
=1:1:2,故化学式为NaCuO2,X与浓盐酸反应,根据反应现象,产物有Cl2,和CuCl2蓝色溶液,因而化学方程式为2NaCuO2+8HCl2NaCl+2CuCl2+Cl2↑+4H2O


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示。下列关于整个反应过程中的叙述错误的是
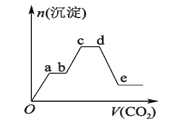
A. Oa段反应的化学方程式是Ba(OH)2+CO2 =BaCO3↓+H2O
B. bc段与cd段所消耗CO2的体积相同
C. bc段反应的离子方程式是2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32-
D. de段沉淀减少是由于BaCO3固体的消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2![]() CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl
CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl![]() C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
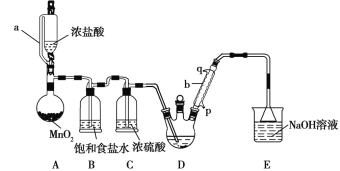
回答下列问题:
(1)用仪器a代替普通分液漏斗的目的是_______________。
(2)装置A中MnO2可以用KMnO4代替,反应可以在常温下进行,试写出反应的离子方程式__。
(3)仪器b中冷凝水从___(填“p”或“q”,下同)口进,___口出。
(4)若撤去装置B,对实验的影响是______________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是___________。
(6)已知:CCl3CHO+OH-![]() CHCl3+HCOO-;HCOO-+I2
CHCl3+HCOO-;HCOO-+I2![]() H++2I-+CO2↑;I2+2S2O32-
H++2I-+CO2↑;I2+2S2O32-![]() 2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
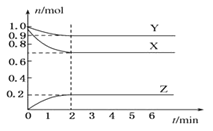
(1)该反应的化学方程式为___。
(2)反应开始至2min,气体Z的平均反应速率为___。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的___倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时 ___(填”增大”“减小”或”相等”)。
③若此时将容器的体积缩小为原来的![]() 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为___反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为___反应(填“放热”或“吸热”)。
(4)在一密闭容器中发生反应N2(g)+3H2(g) ![]() 2NH3(g)△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
2NH3(g)△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
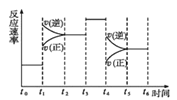
①处于平衡状态的时间段是___(填字母代号)。
A.t0t1 B.t1t2 C.t2t3 D.t3t4 E.t4t5 F.t5t6
②判断t1、t3、t4时刻分别改变的一个条件是:t1时刻___;t3时刻___;t4时刻___。 (填字母代号)
A. 增大压强 B.减小压强 C.升高温度 D. 降低温度 E.加催化剂 F.恒温恒容时充入氮气
③依据上述②中的结论,下列时间段中,氨的百分含量最高的是___(填字母代号)。
A.t0t1 B.t2t3 C.t3t4 D.t5t6。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍 ![]() 是一种重要的化工原料,一种以含镍废料
是一种重要的化工原料,一种以含镍废料![]() 含NiS、
含NiS、![]() 、FeO、CaO、
、FeO、CaO、![]() 为原料制取醋酸镍的工艺流程图如下图所示:
为原料制取醋酸镍的工艺流程图如下图所示:
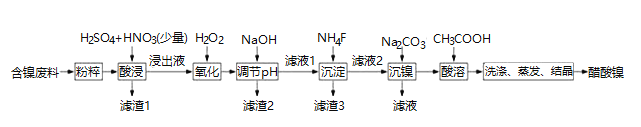
相关离子生成氢氧化物的pH和相关物质的溶解性如表:
金属离子 | 开始沉淀时的pH | 沉淀完全时的pH | 物质 |
|
|
|
|
| 微溶 |
|
|
|
| 可溶 |
|
|
|
| 难溶 |
|
|
|
|
|
![]() 的电子式为_________________。
的电子式为_________________。
![]() 调节pH步骤中,溶液pH的调节范围是_________________。
调节pH步骤中,溶液pH的调节范围是_________________。
![]() 滤渣1和滤渣3主要成分的化学式分别是_________________、_________________。
滤渣1和滤渣3主要成分的化学式分别是_________________、_________________。
![]() 酸浸过程中,lmolNiS失去
酸浸过程中,lmolNiS失去![]() 个电子,同时生成两种无色有毒气体,写出该反应的化学方程式:________。
个电子,同时生成两种无色有毒气体,写出该反应的化学方程式:________。
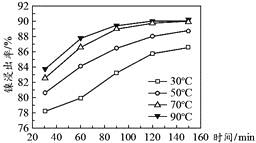
![]() 保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如下图所示,酸浸的最佳温度与时间分别为_________________。
保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如下图所示,酸浸的最佳温度与时间分别为_________________。
![]() 沉镍过程中,若
沉镍过程中,若![]() ,欲使100mL该滤液中的
,欲使100mL该滤液中的![]() 沉淀完全
沉淀完全![]() ,则需要加入
,则需要加入![]() 固体的质量最少为___________
固体的质量最少为___________![]() 保留小数点后2位有效数字
保留小数点后2位有效数字![]() 。
。
![]() 近年来镍氢电池发展很快,它可由
近年来镍氢电池发展很快,它可由![]() 跟
跟![]() 中各元素化合价均可看作是零
中各元素化合价均可看作是零![]() 组成:
组成:![]()
![]()
![]() 。该电池放电时,负极反应是________。
。该电池放电时,负极反应是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中c(OH-)与所加NaOH溶液的体积(V)的关系如图所示。下列说法不正确的是( )
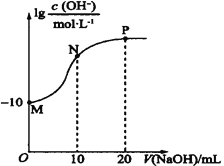
A.常温下,Ka(HA)≈1.0×10-6
B.N点溶液中存在:c(Na+)+c(H+)=c(A-)+c(OH-)
C.P点后的溶液中均存在:c(Na+)>c(A-)>c(OH-)>c(H+)
D.水的电离程度:M<N<P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.恒容密闭容器中的反应3A(g)![]() B(g)+C(g),平衡后再充入少量A气体,A的转化率增大
B(g)+C(g),平衡后再充入少量A气体,A的转化率增大
B.SO2的催化氧化是一个放热的反应,所以升高温度,反应的速率减慢
C.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
D.反应NH3(g)+HCl(g![]() NH4C1(s) ΔH<0,在任何条件下均能自发进行
NH4C1(s) ΔH<0,在任何条件下均能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com