
����Ŀ����ѧ��ȼ�ռ����Ļ���ԭ���ǽ���������(��Fe2O3��FeO��)��ȼ�������ֱ�ӽӴ��Ĵ�ͳȼ�շ�Ӧ�ֽ�Ϊ�������̷�Ӧ��ȼ�����������Ӵ������������������е��������ݸ�ȼ�ϡ��ش��������⣺
(1)��FeO�������������ַ�Ӧ��lgKp���¶ȵĹ�ϵ��ͼ��ʾ������֪��ƽ�ⳣ��Kp����ƽ���ѹ��ƽ���ѹ=��ѹ�����ʵ�������������ƽ��Ũ�ȣ�

��ͼ���漰�ķ�Ӧ�У��������ȷ�Ӧ���Ƿ�Ӧ_________________(����ĸ)��
��R���Ӧ�¶��£���ij�����ܱ�������ͨ��1.5 mol CO��������������FeO��ֻ������ӦCO(g)�� FeO(s) ![]() CO2(g) ��Fe(s)����CO��ƽ��ת����Ϊ______________
CO2(g) ��Fe(s)����CO��ƽ��ת����Ϊ______________
(2)��T���£���ij�����ܱ������м���2 mol CH4(g)��8 mol FeO(s)���з�Ӧ��CH4(g)��4FeO(s) ![]() 4Fe(s)��2H2O(g)��CO2(g)����Ӧ��ʼʱѹǿΪP0���ﵽƽ��״̬ʱ������������ѹǿ����ʼѹǿ��2����
4Fe(s)��2H2O(g)��CO2(g)����Ӧ��ʼʱѹǿΪP0���ﵽƽ��״̬ʱ������������ѹǿ����ʼѹǿ��2����
��T���£��÷�Ӧ��Kp = ______________
������ʼʱ��������м���1molCH4(g)��4molFeO(s)��1mol H2O(g)��0.5molCO2(g)����ʱ��Ӧ��__________________(��������Ӧ�������淴Ӧ��)������С�
�������������䣬������������Ϊ��ѹ�ܱ����������ʱCH4��ƽ��ת����___________(���������� ����С������������)��
(3)һ���������ռ�����úȼ���ŷŵ�CO2��ȫ����Ч�ķ�ʽ�������������ڲ�����Na2CO3��Һ����ԭ����ͼ��ʾ��
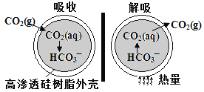
��������������CO2��ԭ����___________________�������ӷ���ʽ��ʾ����
�������չ����е�n(CO2)��n(Na2CO3)=1��3ʱ����Һ��c(CO32��)_____c(HCO3��)������>������ <������=����
�۽��������CO2���������ȡ��ϩ��
��֪��C2H4(g)��3O2(g)=2CO2(g)��2H2O(g) ��H1= -1323kJ��mol-1
2H2(g)��O2(g)=2H2O(g) ��H2= -483.6kJ��mol-1
2CO2(g)��6H2(g)=C2H4(g)��4H2O(g) ��H3=_______________
���𰸡�bc 50% ![]() ����Ӧ ���� CO2 + CO32 + H2O= 2HCO3�� < 127.8kJ��mol1
����Ӧ ���� CO2 + CO32 + H2O= 2HCO3�� < 127.8kJ��mol1
��������
(1)��ͼ���漰�ķ�Ӧ�У���Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����ƽ�ⳣ�������R���ƽ�ⳣ�����ó�c(CO)��c(CO2)��ϵ�����ݹ�ϵ����ת����CO�����ʵ������ټ���CO��ƽ��ת���ʡ�
(2)��������ʽ���ٸ���ѹǿ֮�ȵ����������ʵ���֮�ȣ����ݷ�Ӧ�����ʵ����ܺͼ������������ٸ���ƽ�ⳣ�����м��㣻������Ũ���̽��м�������ƽ�ⳣ���Ƚϣ���������������Ϊ��ѹ�ܱ�������ѹǿ��С��ƽ����������ӷ����ƶ���
(3)����������CO2��ԭ����CO2��Na2CO3��Һ��Ӧ����NaHCO3�����ó���Ӧ����Һ�����ʣ��ٸ���Ũ�ȹ�ϵ��������Ũ�ȴ�С��ϵ������˹���ɷ�������2������ʽ�ӳ���3�ټ�ȥ��1������ʽ��
(1)��ͼ���漰�ķ�Ӧ�У���Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����ƽ�ⳣ�������Ӧbc�����ȷ�Ӧ���ʴ�Ϊ��bc��
��R���Ӧ�¶��£���ij�����ܱ�������ͨ��1.5 mol CO��������������FeO��ֻ������ӦCO(g)�� FeO(s) ![]() CO2(g) ��Fe(s)��lgKp=0��Kp=1����c(CO)= c(CO2)�������ǵ������Ӧ�����ת����CO�����ʵ����������ɵ�CO2�����ʵ���������ʣ���CO�����ʵ�����ת����CO�����ʵ���Ϊ0.75mol����CO��ƽ��ת����Ϊ
CO2(g) ��Fe(s)��lgKp=0��Kp=1����c(CO)= c(CO2)�������ǵ������Ӧ�����ת����CO�����ʵ����������ɵ�CO2�����ʵ���������ʣ���CO�����ʵ�����ת����CO�����ʵ���Ϊ0.75mol����CO��ƽ��ת����Ϊ![]() ���ʴ�Ϊ��50%��
���ʴ�Ϊ��50%��
(2)��T���£���ij�����ܱ������м���2 mol CH4(g)��8 mol FeO(s)���з�Ӧ��CH4(g)��4FeO(s) ![]() 4Fe(s)��2H2O(g)��CO2(g)����Ӧ��ʼʱѹǿΪP0���ﵽƽ��״̬ʱ������������ѹǿ����ʼѹǿ��2��������ѹǿ֮�ȵ������ʵ���֮�ȣ�ѹǿ��ԭ����2���������ʵ���Ϊԭ����2����
4Fe(s)��2H2O(g)��CO2(g)����Ӧ��ʼʱѹǿΪP0���ﵽƽ��״̬ʱ������������ѹǿ����ʼѹǿ��2��������ѹǿ֮�ȵ������ʵ���֮�ȣ�ѹǿ��ԭ����2���������ʵ���Ϊԭ����2����

![]() ��x = 1
��x = 1
��T���£��÷�Ӧ��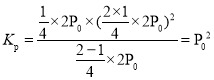 ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
������ʼʱ��������м���1molCH4(g)��4molFeO(s)��1mol H2O(g)��0.5molCO2(g)����ʱ��ѹǿ�ǿ�ʼ��Һѹǿ��![]() ����ʱ
����ʱ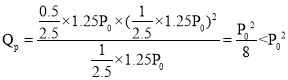 ����Ӧ������Ӧ������У��ʴ�Ϊ������Ӧ��
����Ӧ������Ӧ������У��ʴ�Ϊ������Ӧ��
�������������䣬������������Ϊ��ѹ�ܱ�������ѹǿ��С��ƽ����������ӷ��������ƶ�����CH4��ƽ��ת�������ʴ�Ϊ������
(3)��������������CO2��ԭ����CO2��Na2CO3��Һ��Ӧ����NaHCO3�������ӷ���ʽΪCO2 + CO32 + H2O= 2HCO3�����ʴ�Ϊ��CO2 + CO32 + H2O= 2HCO3����
�������չ����е�n(CO2)��n(Na2CO3)=1��3ʱ����Ӧ����Һ������ΪNa2CO3��NaHCO3������Ũ����ȣ�����CO32ˮ��̶ȴ�������HCO3���������Һ��c(CO32��) < c(HCO3��)���ʴ�Ϊ�� <��
������2������ʽ�ӳ���3�ټ�ȥ��1������ʽ�õ�2CO2(g)��6H2(g)=C2H4(g)��4H2O(g) ��H3=127.8kJ��mol1���ʴ�Ϊ��127.8kJ��mol1��


 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Դ�����ҺΪԭ�ϣ�ͨ�����ķ������Ʊ�С�մ�ԭ��װ��ͼ���£�

����װ�ù���ʱ�������й�˵����ȷ����
A. Na+���ҳش�������Ĥ����׳�
B. �׳ص缫��Ӧ��4CO32-+2H2O-4e-=4HCO3-+O2��
C. �ҳص缫�ӵ������������XΪH2
D. NaOH��ҺY��NaOH��ҺZŨ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ظ������Cr2O72-���������CrO42-�����Ӽ��������ƽ�⣺Cr2O72- +H2O ![]() 2CrO42-+2H+����װ��4mL0.1mol��L-1K2Cr2O7��Һ�м���1mol��L-1��NaOH���Σ���Һ����ɫ��_________ɫ��____________ɫ��ƽ�ⳣ���ı���ʽ�� K= __________________________��
2CrO42-+2H+����װ��4mL0.1mol��L-1K2Cr2O7��Һ�м���1mol��L-1��NaOH���Σ���Һ����ɫ��_________ɫ��____________ɫ��ƽ�ⳣ���ı���ʽ�� K= __________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦCOCl2(g)![]() CO(g)��Cl2(g) ��H>0���ﵽƽ��ʱ�����д�ʩ��
CO(g)��Cl2(g) ��H>0���ﵽƽ��ʱ�����д�ʩ��
������ �ں���ͨ��������� ������COŨ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ��ǣ� ��
A.�٢ڢ�B.�٢ܢ�C.�ڢۢ�D.�ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ѧ���������ҹ������������������ƣ�Na2S2O8������SΪ��6�ۣ�ȥ����ˮ�е�+5����[As(V)]�Ŀ��гɹ�����Ӧ������ͼ����NAΪ�����ӵ�������ֵ��Ksp[Fe(OH)3]=2.7��10-39������������ȷ����
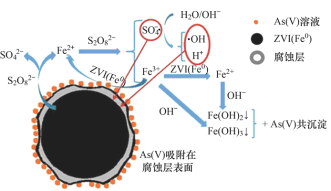
A.1mol��������(Na2S2O8)��2NA��������
B.��56gFe�μӷ�Ӧ������1.5NA��S2O82-����ԭ
C.���������£���������ɻ�������Ӧ�ķ���ʽΪ��SO4-��+ OH- ��SO42- +��OH
D.�����£�pHԽ��Խ������ȥ����ˮ�е�+5���飬��Һ��c(Fe3+)Ϊ2.7��10-27mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ���������Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ������˵���������
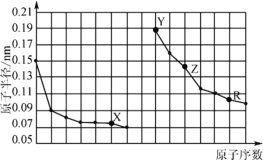
A.X��R������ϼ���ͬ
B.������ڵ�X��Z���ɵĻ�������Եõ�����Z
C.X��Y�γɵĻ��������������������ӵĸ�����һ����2:1
D.Y��Z��R��Ӧ������������ˮ�����֮����Է�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ����(����)
A.��0.1 mol��L��1 CH3COOH��Һ�м�������ˮ����Һ�� ����
����
B.��CH3COONa��Һ��20 ��������30 ������Һ��![]() ����
����
C.�������м��백ˮ�����ԣ���Һ��![]() >1
>1
D.0.1 mol AgCl��0.1 mol AgI��Ϻ����1 Lˮ��������Һ��c(Cl��)��c(I��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ���

��1������ȼ�ϵ�ص�����ת����Ҫ��ʽ��___���ڵ����е�����������Ϊ___(��a��b�ͼ�ͷ��ʾ)��
��2��������Ӧ�ĵ缫��Ӧ����ʽΪ___��
��3���������Ʊ��ʹ洢������ȼ�ϵ���ܷ���Ч�ƹ�Ĺؼ�����������������ù������װ�õ�����صļ�����Һ���Ʊ���������������ǵ�����������̫��������Ҫ��ʽ֮һ��ͼ1Ϊ�����������װ�ã�ͼ2Ϊ�������[CO(NH2)2](CΪ��4��)�ļ�����Һ�����װ��ʾ��ͼ(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)��

��ͼ1��N�Ͱ뵼��Ϊ___(�������������)
�ڸ�ϵͳ����ʱ��A���ĵ缫��ӦʽΪ___��
����A������7.00gN2�����ʱB������___LH2(��״����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����0.8 mol H2��0.6 mol I2����һ�������·�����Ӧ��H2(g)+I2(g)2HI(g)��H<0����Ӧ�и����ʵ����ʵ�����ʱ��仯�����ͼ��
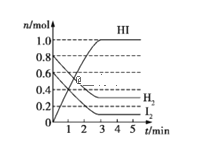
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ______���������¶ȣ���ѧƽ�ⳣ��K______(����������������С������������)��
(2)����ͼ�����ݣ���Ӧ��ʼ���ﵽƽ��ʱ��ƽ������v(HI)=_____mol��L-1��min-1��ת������(H2)=_____��
(3)HI�����������(HI)��ʱ��仯��ͼ�����ߢ���ʾ�����ı䷴Ӧ�������ڼ���������(HI)�ı仯��ͼ�����ߢ���ʾ��������������(HI)�ı仯��ͼ�����ߢ���ʾ���������������_____(����������������ţ���ͬ)��������������______��
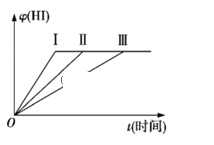
�ٺ��������£������¶�
�ں��������£������¶�
�ۺ��������£���С��Ӧ�������
�ܺ��������£�����Ӧ�������
�ݺ��º��������£������ʵ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com