
(1)核电荷数是3,核外电子数是2。
______________________________________________________________________________
(2)最外层电子数是次外层电子数的3倍。
______________________________________________________________________________
(3)核内有10个质子,相对原子质量为20的原子。
______________________________________________________________________________
(4)核内只有一个质子的阴离子。
______________________________________________________________________________
(5)有3个电子层,失去2个电子呈中性的粒子。
______________________________________________________________________________
科目:高中化学 来源: 题型:
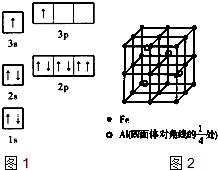 (1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:| 电离能(kJ?mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
| 3 |
| ||
| 3 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
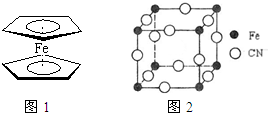 铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂.
铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂. )中含有σ键的数目为
)中含有σ键的数目为查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 电离能(kJ-mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
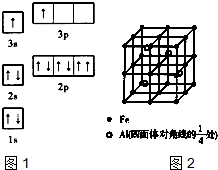
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
 [Cu(NH3)4]2++2OH-+
[Cu(NH3)4]2++2OH-+
查看答案和解析>>
科目:高中化学 来源:2012-2013学年宁夏银川一中高三(上)期中化学试卷(解析版) 题型:解答题
| 电离能 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com