

分析 (1)催化剂改变反应速率不改变化学平衡;
(2)①平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;
②图象读取甲醇生成浓度,结合反应速率概念计算甲醇的反应速率,依据反应速率之比等于化学方程式计量数之比得到氢气反应速率;
③反应焓变是指1mol二氧化碳和3mol氢气完全反应放出的热量为49KJ,反应是可逆反应,在体积为1L的密闭容器中,充入1molCO2和3molH2,反应放热一定小于49KJ,结合图象中二氧化碳转化率计算此时达到平衡放出的热量,在相同条件下,密闭容器的体积缩小至0.5L时,压强增大,平衡正向进行,反应放出热量会增多;
④反应是气体体积减小的放热反应,升温平衡逆向进行,增大压强平衡正向进行,据此分析图象确定表示的物理量;
(3)根据题意知,该反应是可逆反应,反应物是硫化氢,根据图象知,生成物中含有S元素的物质是氢气的一半,则生成物是S2和H2,再结合反应条件书写方程式;(5)①由电池装置图可知,Cu上二氧化碳得电子生成甲烷;
②根据酸的挥发性分析;
(4)反应Ⅰ的热化学方程式可以依据反应Ⅱ、Ⅲ热化学方程式计算得到,同时得到反应的焓变;
(5)还原性Fe>Cu,则稀硝酸不足时铁优先反应生成硝酸亚铁:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,若硝酸有剩余,则铜参与反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,若硝酸足量,则亚铁离子被氧化生成铁离子,发生总反应为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,据此对各选项进行判断.
解答 解:(1)将煤转化成水煤气的反应:C(s)+H2O?CO2(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),催化剂改变反应速率不改变化学平衡,不改变反应焓变,此反应的△H不变,加入催化剂后反应物和生成物的总能量不变
故答案为:不变;加入催化剂后反应物和生成物的总能量不变;
(2)①CO2(g)+3H2(g)?CH3OH(g)+H2O(g),反应的平衡常数表达式为:K=$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{c(CO){c}^{3}({H}_{2})}$,
故答案为:$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{c(CO){c}^{3}({H}_{2})}$;
②图象读取甲醇生成浓度,结合反应速率概念计算甲醇的反应速率=$\frac{0.75mol/L}{9min}$,反应速率之比等于化学方程式计量数之比,V(H2)=3V(CH3OH(g)=3×$\frac{0.75mol/L}{9min}$=0.25mol/L•min,
故答案为:0.25mol/L•min;
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,反应达到平衡状态消耗二氧化碳物质的量浓度=1mol/L-0.25mol/L=0.75mol/L,物质的量为0.75mol,反应放出热量=49KJ/mol×0.75mol=36.75KJ,反应焓变是指1mol二氧化碳和3mol氢气完全反应放出的热量为49KJ,反应是可逆反应,在体积为1L的密闭容器中,充入1molCO2和3molH2,反应放热一定小于49KJ,在相同条件下,密闭容器的体积缩小至0.5L时,压强增大,平衡正向进行,反应放出热量会增多,大于36.75KJ,则36.75<Q<49,
故答案为:c;
④CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,反应是气体体积减小的放热反应,
i.温度升高,平衡逆向进行,二氧化碳转化率减小,所以X为温度,L为压强,
故答案为:温度;
ii.温度一定压强增大平衡正向进行二氧化碳转化率增大,所以L1>L2,
故答案为:L1>L2;
(3)由电池装置图可知,Cu上二氧化碳得电子生成甲烷,则Cu电极上的电极反应为:CO2+8e-+8H+=CH4+2H2O,可向装置中加入少量的酸作电解质,由于盐酸易挥发,生成的甲烷中会混有HCl气体,所以选用硫酸,不用盐酸
故答案为:CO2+8e-+8H+=CH4+2H2O;硫酸;
(4)反应Ⅰ:2NH3(g)+CO2(g)?NH2COONH4(s)△H1=akJ•mol-1
反应Ⅱ:NH2COONH4(s)?CO(NH2)2(s)+H2O(g)△H2=+72.49kJ•mol-1
总反应Ⅲ:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H3=-86.98kJ•mol-1
依据盖斯定律计算反应Ⅰ+反应Ⅱ得到:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)△H3=akJ•mol-1+72.49kJ•mol-1=-86.98kJ•mol-1
a=-159.47akJ•mol-1,
故答案为:-159.47KJ/mol;
(5)A.若剩余金属0.5a mol,该金属可能为铁或铜,若为铁,则溶质为硝酸亚铁,若为铜,则氧化产物可能为硝酸亚铁和硝酸铜,故A正确;
B.若只有一种氧化产物,说明铁过量,铜没有参与反应,反应后溶质为硝酸亚铁,但是amol铁不一定完全反应,无法确定a与c的关系,故B错误;
C.若只有二种氧化产物,氧化产物可能为硝酸亚铁和硝酸铜或硝酸铜和硝酸铁,硝酸可能过量,稀硝酸不一定完全反应,则无法计算被还原的硝酸的量,故C错误;
D.若有三种氧化产物,氧化产物为硝酸铜、硝酸铁和硝酸亚铁,说明硝酸完全反应,根据反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O、Fe+4HNO3=Fe(NO3)3+NO↑+2H2O可知,被还原的硝酸的物质的量为cmol×$\frac{1}{4}$=0.25cmol,故D正确;
故答案为:BC.
点评 本题考查了原电池原理、方程式的书写、化学平衡常数、平衡移动等,题目涉及的知识点较多,侧重于考查学生对基础知识的综合应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2 $\stackrel{光照}{→}$ CH3Cl+HCl | B. | CH2═CH2+Br2→CH2BrCH2Br | ||
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | D. | 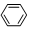 +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{50~60℃}^{浓H_{2}SO_{4}}$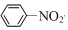 +H2O +H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 利用图1装置可定量测定H2O2的分解速率 | |
| B. | 图2中E1表示使用催化剂后的反应热 | |
| C. | 图3表示在平衡体系FeCl3+3KSCN?Fe(SCN)3+3KCl的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图象 | |
| D. | 图4表示弱电解质在水中建立电离平衡的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:3 | C. | 2:3 | D. | 4:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入AgNO3溶液,可生成白色沉淀,加稀盐酸沉淀不消失,则可确定该溶液中一定含有Cl-, | |
| B. | 用试管加热碳酸氢钠固体时试管口竖直向上 | |
| C. | 实验室需要800mL0.1mol•L-1NaOH溶液,需要称取4.0gNaOH进行配制 | |
| D. | 实验室中可用碱石灰干燥氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾溶于水产生具有吸附性的胶体粒子,可杀菌消毒 | |
| B. | 氯水可使有色布条褪色,说明氯气具有漂白性 | |
| C. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| D. | 碳素钢和光导纤维都属于新型的无机非金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com