
| A.2 | B.3 | C.12 | D.14 |
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
| A.11∶1 | B.9∶1 | C.1∶11 | D.1∶9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-) |
| C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D.d点:c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3溶液中:c(H+) + c(Na+)=c(HCO3-)+2c(CO32-) + c(OH-) |
| B.pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)一样多 |
| C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
| D.向10 mL 0.10mol?L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1×10—14 | B.大于1×10—14 | C.小于1×10—14 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.前者减小后者不变 | B.前者减小后者增大 | C.都不变 | D.都减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
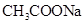 与
与 ②
② 与NaOH ③
与NaOH ③ 与
与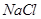 ④
④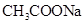 与
与 ,下列各项排序正确的是
,下列各项排序正确的是| A.pH:②>③>④>① | B. :②>④>③>① :②>④>③>① |
| C.溶液中c(H+): ①>③>②>④ | D.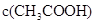 : ①>④>③>② : ①>④>③>② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.③② | C.④ | D.③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com