
【题目】下列说法中不正确的是
A. 金属的冶炼原理,就是在一定条件下将金属从其化合物中还原出来
B. 将少量Na放入硫酸铜溶液中,可生成金属铜
C. 将废铁屑加入FeCl2溶液中,可用于除去工业废气中的Cl2
D. 铝合金可大量用于高铁建设
科目:高中化学 来源: 题型:
【题目】实验测得1mol H2与1mol Cl2反应生成2mol HCl时,放出184.6kJ的热量,其理论分析数据与实验数据略有差异,如图表示上述反应能量变化的理论分析示意图:
(1)化学键断裂需要(填“释放”或“吸收”)能量;
(2)图中表示了吸收和释放的能量,其中释放的能量共kJ;
(3)该反应的反应物的总能量(填“大于”、“等于”或“小于”)反应产物的能量,所以该反应是(填“放热”或“吸热”)反应;
(4)用图示数据计算其反应热,写出该反应的热化学方程式 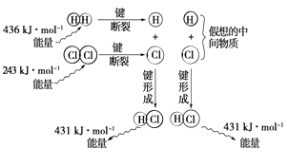
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2混合气体3 g和足量的氧气燃烧后,在150℃时将混合气体通过足量的Na2O2后,Na2O2增重的质量为
A.1.5 g B.3 g C.6 g D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
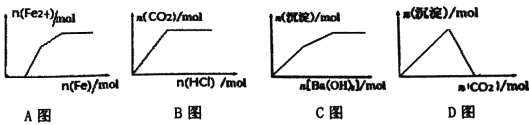
A. Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉
B. Na2CO3、NaHCO3溶液中逐滴加入HCl
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
D. NaAlO2溶液中逐渐通入CO2
【答案】A
【解析】A.Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉,铁粉先和稀硝酸完全反应生成Fe(NO3)3,继续加入铁粉,将溶液里的Fe(NO3)3全部还原为Fe(NO3)2,最后与Cu(NO3)2反应生成Cu和Fe(NO3)2,故A正确;B.Na2CO3、NaHCO3溶液中逐滴加入稀HCl,先与Na2CO3反应生成NaHCO3,完全反应后继续滴加稀盐酸,NaHCO3与稀HCl反应生成CO2气体,故B错误;C.假设n(KAl(SO4)2)=2mol,则n(Al3+)=2mol,n(SO42-)=4mol,当加入n(Ba(OH)2)=3mol时,Al3+完全沉淀生成2mol Al(OH)3,此时SO42-剩余1mol,继续加入1mol Ba(OH)2,此时发生的反应为Ba2++SO42-═BaSO4、Al(OH)3+OH-═AlO2-+2H2O,生成1molBaSO4沉淀,同时有2molAl(OH)3溶解,因此沉淀的物质的量减少,最后保持不变,根据分析可知图象应该只有一段上升的过程,故C错误;D.NaAlO2溶液中通入CO2,开始出现沉淀,当CO2过量时沉淀不溶解为定值,故D错误;故答案为A。
【题型】单选题
【结束】
16
【题目】下列实验中,对应的现象及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 向FeSO4溶液中滴加HNO3酸化的H2O2 | 溶液由浅绿色变为黄色 | 氧化性: H2O2>Fe3+ |
B | 将铜粉加入lmol/LFe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 活泼性: Fe>Cu |
C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 金属熔化,液态铝不滴落下来 | 熔点: A12O3>A1 |
D | 向饱和NaHCO3溶液中滴加浓盐酸,再将产生的气体通入NaAlO2溶液 | NaAlO2 溶液变浑蚀 | 酸性: HCl>H2CO3>Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是
A. K+、Fe2+、MnO4-、H+B. Fe3+、SCN-、Cl-、K+
C. Ba2+、Na+、SO32-、OH-D. NH4+、SO42-、OH-、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应的中和热为 , 表示该中和热的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能增大相应化学反应速率的是( )
A. 盐酸和大理石反应制取CO2时,增加大理石的用量
B. Cu与稀硝酸反应制取NO时,改用浓硝酸
C. NH4Cl与熟石灰反应制NH3时,增大压强
D. 在用Zn和稀硫酸反应制氢气时,加入几滴硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com