
分析 (1)依据热化学方程式和盖斯定律计算得到所需热化学方程式,反应自发进行的判断依据是△H-T△S<0;
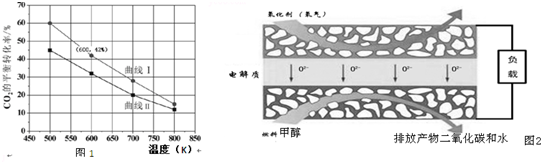
(2)①图象分析相同温度下,两种反应物,增大一种物质的量会提高另一种物质的转化率;
②结合三行式进行计算,化学反应的平衡常数K各个生成物平衡浓度系数次方的乘积和各个反应物平衡浓度系数次方乘积的比值,据此计算;计算Qc判断Qc与K的大小关系确定反应进行方向; CO2(g)+3H2(g)?CH3OH(g)+H2O(g)为气体系数减小的反应,若为恒容容器随着反应进行,容器内压强减小,若为恒压容器,随着反应进行容器体积偏小,相当于在恒容仪器条件下加压,依据压强对化学平衡移动的影响,判断平衡移动的方向及二氧化碳转化率;
(3)①以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,分析该电池的工作原理如图3所示可知负极是甲烷失电子发生氧化反应,结合导电离子和电荷守恒分析书写;
②依据电极反应计算转移电子物质的量,阴极生成氢气的物质的量和标况下体积.
解答 解:(1)反应Ⅰ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)?CO (g)+H2O(g)△H2
反应Ⅲ:CO(g)+2H2(g)?CH3OH(g)△H3=-90.77kJ•mol-1
根据盖斯定律,反应Ⅱ可以是Ⅰ-Ⅲ得到,所以反应Ⅱ的焓变△H2=(-49.58kJ•mol-1)-(-90.77kJ•mol-1)=+41.19 kJ•mol-1;根据反应自发行的判据:△H-T△S<0,反应Ⅲ是熵减的放热的反应,所以要自发进行需要在较低温下进行,
故答案为:+41.19 kJ•mol-1;较低温;
(2)①A:n(H2)=3mol,n(CO2)=1.5mol,B:n(H2)=3mol,n(CO2)=2mol,二者比较B相当于增大二氧化碳的量,转化率小于A,所以曲线 I代表A的投料,
故答案为:A;
②在温度为500K的条件下,充入3mol H2和1.5mol CO2,该反应10min时达到平衡,二氧化碳的转化率是60%,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
初始浓度:0.5 1 0 0
变化浓度:0.3 0.9 0.3 0.3
平衡浓度:0.2 0.1 0.3 0.3
a.该温度下,反应I的平衡常数K=$\frac{0.3×0.3}{0.2×0.1{\;}^{3}}$=450;
若在此容器中开始充入0.3molH2和0.9mol CO2、0.6molCH3OH、0.6molH2O,则各种气体的分别浓度为:0.1mol/L,0.3mol/L,0.2mol/L,0.2mol/L,
则:Qc=$\frac{0.2×0.2}{0.3×0.1{\;}^{3}}$=133.3,Qc<K,所以平衡正向移动;
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)为气体系数减小的反应,若为恒容容器随着反应进行,容器内压强减小,若为恒压容器,随着反应进行容器体积偏小,相当于在恒容仪器条件下加压,加压平衡向气体系数和减小的反应,即正向移动,则消耗的二氧化碳增多,二氧化碳的转化率大于60%;
故答案为:450;正;大于;
(3)①以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,分析该电池的工作原理如图2所示可知负极是甲烷失电子发生氧化反应,结合导电离子和电荷守恒分析书写电极反应为:CH3OH-6e-+3O2-=CO2↑+2H2O,
故答案为:CH3OH-6e-+3O2-=CO2↑+2H2O;
②16g甲醇物质的量=$\frac{16g}{32g/mol}$=0.5mol,发生反应时电子转移0.5mol×6=3mol,依据2H+~2e-~H2↑,则生成氢气的物质的量为:$\frac{3mol}{2}$=1.5mol,标况下体积为:1.5mol×22.4L/mol=33.6L;
故答案为:33.6.
点评 本题综合考查学生盖斯定律的应用、化学反应速率的计算、化学平衡移动的影响因素、电化学等知识,属于综合知识的考查,难度较大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某烷烃的命名为:2-甲基-3-乙基丁烷 | |
| B. | 分子式为 C4H8O2的酯有 4 种 | |
| C. | 乙烯分别使溴水和酸性 KMnO4 溶液褪色,反应类型相同 | |
| D. | 油脂是能发生水解反应的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
下列溶液中,K+的物质的量浓度最大的是( )
A.0.1 mol/L的KNO3 溶液500 ml B.0.05mol/L的K2SO4 溶液300ml
C.0.04mol/L的K3PO4 溶液100 ml D.0.06mol/L的KHCO3 溶液120 ml
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应Ⅰ是氧化还原反应,反应Ⅱ是非氧化还原反应 | |
| B. | H3PO2具有还原性,在空气中可能被氧化成磷酸 | |
| C. | 反应Ⅰ中氧化剂与还原剂的质量之比为1:1 | |
| D. | 反应Ⅰ中,在标准状况下生成2.24 L PH3时,转移0.3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA | |
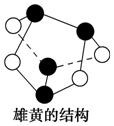
| B. | 0.5 mol雄黄(As4S4,所有原子都满足8电子结构,结构如图)含有NA个S-S键 | |
| C. | 39 g苯分子中共含6 NA个共价单键 | |
| D. | 向FeI2、NaBr的混合溶液中通入适量氯气,当有1 molFe2+被氧化时,该反应转移电子的数目至少为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com