
【题目】A、B、C、D、E、F六种物质的转化关系如图所示。
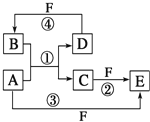
(1)若 A 为短周期金属单质,D 为短周期非金属单质,且所含元素的原子序数 A 是 D 的 2 倍,所含元素的原子最外层电子数 D 是 A 的 2 倍,F 的浓溶液与 A、D 反应都有红棕色气体生成。请写出以下物 质的化学式:B_____F_____;反应④的化学方程式为_____.
(2)若 A 是常见的变价金属的单质,D、F 是气态单质,且反应①在水溶液中进行。反应②也在水溶液 中进行,其离子方程式是_____。
【答案】CO2 HNO3 C+4HNO3(浓)=CO2↑+4NO2↑+2H2O Cl2+2Fe2+=2Cl-+2Fe3+
【解析】
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,则A是Mg、D是C元素;F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2,A是Mg,反应④的化学方程式为在加热条件下,碳和浓硝酸发生氧化还原反应生成二氧化碳、二氧化氮和水,反应方程式为:C+4HNO3(浓)![]() CO2+4NO2↑+2H2O,故答案为:CO2;HNO3;C+4HNO3(浓)
CO2+4NO2↑+2H2O,故答案为:CO2;HNO3;C+4HNO3(浓)![]() CO2+4NO2↑+2H2O;
CO2+4NO2↑+2H2O;
(2)若A是常见的变价金属的单质,则A是Fe,D、F是气态单质,反应①在水溶液中进行.反应②也在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2,氯化亚铁被氯气氧化生成氯化铁,离子反应方程式为:Cl2+2Fe2+=2Cl-+2Fe3+,故答案为:Cl2+2Fe2+=2Cl-+2Fe3+。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】用甲苯合成某保湿香料E的流醒如下:

已知:在稀碱溶液中,若环上的卤素原子不易发生取代
(1)上述流程中属于取代反应的步骤有_______________。
(2)上述流程中加人的试剂:②是________、③是_______、④是________。
(3)B的结构简式是_______________。
(4)下列有关D的叙述正确的是_______(填字母)
A.有两种官能团,是羟基和羧基
B.能在Cu催化剂、加热条件下发生氧化反应
C.可以形成高分子化合物
D.与浓溴水反应产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.若把H2S分子写成H3S分子,违背了共价键的饱和性
B.H3O+离子的存在,说明共价键不应有饱和性
C.所有共价键都有方向性
D.两个原子之间形成共价键时,可形成多个σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 四种常见元素,其中 X、Y、Z 为短周期元素。有关信息如下:
原子或分子相关信息 | 单质及其化合物相关信息 | |
X | ZX4分子是由粗 Z 提纯 Z 的中间产物 | X 的最高价氧化物对应的水化物为无机酸中最强酸 |
Y | Y 原子的最外层电子数等于电子层数 | Y 的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
Z | Z 原子的最外层电子数是次外层电子数的 1/2 | Z 是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
W | W 原子的最外层电子数小于 4 | W 的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1) W 在周期表的位置为________________,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为_________________________。
(2)X 的最高价氧化物对应水化物的水溶液与 Y 的氧化物反应的离子方程式为_________________________。
(3) Z 的氧化物在通讯领域用来作__________________________________________,工业上制备 Z 的单质的化学反应方程式 为___________________________________________ 。锗与 Z 是同一主族元素,门捷列夫曾预言了这一元素的存在,它用 来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH 溶液反应但在有H2O2存在时可与 NaOH 溶液反应生成锗酸盐,其方程式为_________________________。
(4)在50mL1mol·L-1的YX3溶液种逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能___________种情况(填一或二)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是( )
A.胶体能发生电泳现象
B.胶体能产生丁达尔现象
C.胶体粒子直径在1~100nm之间
D.胶体在一定条件下能聚沉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图所示装置检验乙烯时不需要除杂的是
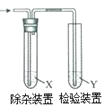
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法不正确的是
A. 相同条件下的沸点:丙三醇>乙二醇>乙醇>乙烷>甲烷
B. 将浸透了石蜡油的石棉放在大试管底部,大试管中加入碎瓷片,加强热,将产生的气体持续通入溴的四氯化碳溶液中,红棕色逐渐变浅,最终褪色
C. —C3H7和—C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种
D. 薄荷醇![]() 中至少有12个原子共平面
中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期主族元素的原子序数依次增大,已知:
①其原子半径大小关系是D>E>B>C>A;
②A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加;
③C是地壳中含量最多的元素,D与C可形成原子个数比为1∶1或2∶1的化合物。
请填写以下空白:
(1)单质B的电子式为____________,结构式为____________。
(2)化合物D2C2的电子式为________________。用电子式表示D2C的形成过程:__________________________。
(3)单质A和单质B在一定条件下发生反应的化学方程式为_________________。
(4)单质E与A、C、D三种元素形成的化合物发生反应的化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com