
���� ��һ���¶��£���2.4molA��1.2molB�����������Ϻ����ݻ�Ϊ2L��ij�ܱ������У�2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������CΪ0.4mol/L��2=0.8mol����
A��g��+B��g��?xC��g��+D��g��
��ʼ����mol����2.4 1.2 0 0
�仯����mol����0.8 0.8 0.8 0.8
ƽ������mol����1.6 0.4 0.8 0.8
��1�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���x=1������v=$\frac{��c}{��t}$����v��B����
��2������A��ת����=$\frac{{n}_{����}��A��}{{n}_{��}��A��}$��100%���м��㣻
��3����ѧƽ�ⳣ����ָ��һ���¶��£����淴Ӧ����ƽ��ʱ���������Ũ��ϵ������֮���뷴Ӧ���Ũ��ϵ������֮���ıȣ����塢��Һ�岻��Ҫ�ڻ�ѧƽ�ⳣ����д��������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ����С��
��� �⣺��һ���¶��£���2.4molA��1.2molB�����������Ϻ����ݻ�Ϊ2L��ij�ܱ������У�2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������C�����ʵ���Ϊ��0.4mol/L��2=0.8mol����
A��g��+B��g��?xC��g��+D��g��
��ʼ����mol��2.4 1.2 0 0
�仯����mol��0.8 0.8 0.8 0.8
ƽ������mol��1.6 0.4 0.8 0.8
��1�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�����0.8mol��0.8mol=x��1����ã�x=1��
2min��v��B��=$\frac{\frac{0.8mol}{2L}}{2min}$=0.2mol/��L•min����
�ʴ�Ϊ��1��0.2mol/��L•min����
��2���ﵽƽ��ʱA��ת����Ϊ��$\frac{0.8mol}{2.4mol}$��100%=33.3%��
�ʴ�Ϊ��33.3%��
��3��A��g��+B��g��?xC��g��+D��g���Ļ�ѧƽ�ⳣ������ʽK=$\frac{c��C��•c��D��}{c��A��•c��B��}$��
����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ����С��450��ʱƽ�ⳣ������500��ʱƽ�ⳣ����
�ʴ�Ϊ��$\frac{c��C��•c��D��}{c��A��•c��B��}$�����ڣ�
���� ���⿼���˻�ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ��漰��Ӧ���ʡ�ת���ʡ���ѧƽ�ⳣ������ѧƽ�⼰��Ӱ���֪ʶ����ȷ����ʽ�ڻ�ѧƽ������е�Ӧ�÷���Ϊ���ؼ�������������ѧ���ķ�����������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MnO4-��Mn2+ | B�� | H2O2��H2O | C�� | H2��H2O | D�� | Zn��Zn2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʴʱ�����ų�O2 | |
| B�� | ���ⸯʴʱ�����ų�H2 | |
| C�� | ���ⸯʴ��������ʴ�ձ� | |
| D�� | ���ⸯʴ��������ʴ�ĸ�����Ӧ����Fe-3e-=Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
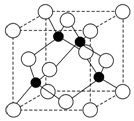 ��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ����ֻ��ϼۣ�����A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺
��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ����ֻ��ϼۣ�����A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
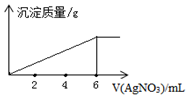
| A�� | +1 | B�� | +2 | C�� | +3 | D�� | +4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com