
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现将氢气和氮气充入某密闭容器中,在一定条件下反应的有关数据为:
| 项目 | H2 | N2 | NH3 |
| 起始时 | 5 mol·L-1 | 3 mol·L-1 | 0 |
| 2 s末 | 2 mol·L-1 |
(1)氢气和氮气反应生成氨气(在2 s内)的反应速率v(H2)=__________。若此时已达平衡,则可求得平衡常数为__________。
(2)下图表示合成NH3反应在时间t0→t6中反应速率与反应过程曲线图,则在下列达到化学平衡的时间段中,化学平衡常数最大的一段时间是__________。
①t0→t1 ②t2→t3 ③t3→t4 ④t5→t6
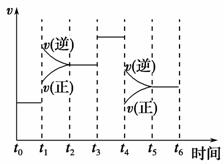
若t1时改变的条件是升高温度,则说明合成NH3反应的焓变ΔH________0(填“大于”或“小于”)。
解析 (1)根据合成氨反应3H2(g)+N2(g)2NH3(g)和表中数据,计算得v(H2)=1.5 mol·L-1·s-1,达到平衡时各物质的浓度分别为n(H2)=2 mol·L-1,n(N2)=2 mol·L-1,n(NH3)=2 mol·L-1,即可求出平衡常数为0.25。
(2)由图可知,从t1开始是化学反应速率增大,而逆反应速率大于正反应速率,说明平衡向左移动,化学平衡常数减小;从t3开始是反应速率增大,平衡不移动,平衡常数相等;从t4开始是化学反应速率减少,而逆反应速率减小的少,大于正反应速率,平衡向左移动,平衡常数减小,故化学平衡常数最大的一段是t0~t1。
升高温度,平衡向左移动,故正向是放热反应ΔH<0。
答案 (1)1.5 mol·L-1·s-1 0.25 (2)① 小于


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
有机物的结构可用键线式简化表示,如CH3—CH==CH—CH3可表示为 ,有一种有机物X的键线式如图所示。
,有一种有机物X的键线式如图所示。

(1)X的分子式为________。
(2)有机物Y是X的同分异构体,且属于芳香族化合物。则Y的结构简式是______________________________________。
(3)Y在一定条件下可发生反应生成高分子化合物,该反应类型属于_______________________________________。
(4)Y可以与溴水反应,该反应的化学方程式是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向10 mL 0.1 mol·L-1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL。下列叙述正确的是 ( )。
A.x=10时,溶液中有NH 、Al3+、SO
、Al3+、SO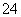 ,且c(NH
,且c(NH )>c(Al3+)
)>c(Al3+)
B.x=10时,溶液中有NH 、AlO
、AlO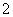 、SO
、SO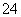 ,且c(NH
,且c(NH )>c(SO
)>c(SO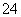 )
)
C.x=30时,溶液中有Ba2+、AlO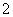 、OH-,且c(OH-)<c(AlO
、OH-,且c(OH-)<c(AlO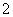 )
)
D.x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-)=c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
请按要求回答下列问题:
(1)已知25 ℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为____________________________。
(2)25 ℃时,向0.01 mol·L-1的MgCl2溶液中,逐滴加入浓NaOH溶液,刚好出现沉淀时,溶液的pH为________;当Mg2+完全沉淀时,溶液的pH为________(忽略溶液体积变化,已知lg 2.4=0.4,lg 7.7=0.9)。
(3)已知25 ℃时,Ksp(AgCl)=1.8×10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag+)约为______ mol·L-1。
(4)已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨时既要使氨的产率增大,又要使反应速率加快,可采取的办法是
( )。
①减压 ②加压 ③升温 ④降温 ⑤及时从平衡混合气中分离出NH3
⑥补充N2或H2 ⑦加催化剂 ⑧减小N2或H2的量
A.③④⑤⑦ B.①②⑤⑥
C.②⑥ D.②③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语以及化学基本概念的表述中正确的一组是
A. 过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同,两者互为同分异构体
B. 日本福岛核电站泄露的放射性核素 Ⅰ和
Ⅰ和 Cs,前者比后者少4个中子
Cs,前者比后者少4个中子
C. 亚硫酸氢钠和碳酸氢钠的电离方程式都表示为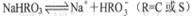
D. 次氯酸的结构式为HOCl,过氧化氢的电子式为
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
| 元素编号 | 元素性质或原子结构 |
| X | 形成的简单阳离子核外无电子 |
| Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z | 元素在周期表的族序数等于周期序数的3倍 |
| T | 同周期元素中形成的简单离子半径最小 |
下列说法正确的是
A. 原子半径大小顺序:T>Z>Y>X
B. X分别与Y、Z均可形成既含极性键又含非极性键的化合物
C. T的单质与Y的最高价氧化物对应水化物的溶液不反应
D. 由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中,只有氧化性、只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
A.F2、K、HCl B.Cl2、Al、H2 C.NO2、Na、Br2 D.O2、SO2、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质溶液的说法正确的是( )
A.将Ca(ClO)2、Na2SO3、FeCl3溶液蒸干均得不到原溶质
B.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解
C.室温下,向0.1mol/L的CH3COOH溶液中加入少量水溶液显碱性的物质,CH3COOH的电离程度一定增大
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com