
| A.向某溶液中加稀盐酸,将产生的无色气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有CO32-或HCO3- |
| B.向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- |
| C.向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则原溶液中存在NH4+ |
| D.向某溶液中加入硝酸银溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Cl- |
 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源:不详 题型:填空题
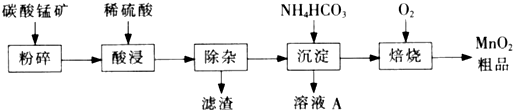 有关氢氧化物开始沉淀和沉淀完全的pH如下表:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:| 氢氧化物 | Al(OH)2 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
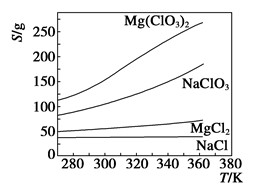
| A.将NaCl溶液蒸干可得NaCl固体 |
| B.将MgCl2溶液蒸干可得MgCl2固体 |
| C.Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯 |
| D.可用MgCl2和NaClO3制备Mg(ClO3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验操作 |
| A | 证明乙烯能发生加成反应 | 将乙烯气体通入溴的四氯化碳溶液中 |
| B | 鉴别Fe(OH)3胶体和FeCl3溶液 | 用激光笔分别照射两种物质,从侧面观察是否出现光亮的通路。 |
| C | 检验酒精中是否含有水 | 取少量酒精加入无水硫酸铜粉末 |
| D | 鉴别苯、环已烯和已烷 | 加入酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | 淀粉(NaCl) | 水 | 过滤 |
| B | BaCO3(BaSO4) | 饱和Na2CO3溶液 | 搅拌、过滤 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 氯化氢(Cl2) | 饱和食盐水 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
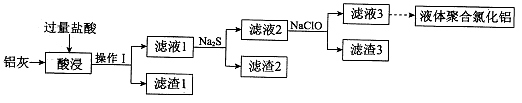


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
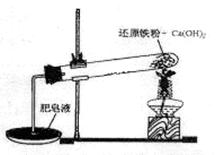
| 操作 | 现象 | 结论 |
| | | 假设一不成立 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com