
两种金属粉末混合物13g,投入足量的稀硫酸中,在标准状况下产生11.2L气体,则这种混合物可能是( )
A.Zn和Cu B.Fe和Zn C.Al和Fe D.Fe和Cu
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:013
由两种金属粉末组成的混合物3.0g,与足量的稀H2SO4反应,生成1.12L H2(标况),则该金属粉末混合物在下列中不可能组成的一组是
[ ]
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:021
将1.5g两种金属的混合物粉末与足量的稀盐酸反应,反应完全后,得到标准状况下的氢气1.12L,则两种金属可能是
[ ]
查看答案和解析>>
科目:高中化学 来源:百练一胜(高一上) 题型:021
将两种金属粉末组成的混合物50g与氯气完全反应,消耗氯气1.0mol,此混合物可能是
[ ]
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:021
将1.5g两种金属的混合物粉末与足量的稀盐酸反应,反应完全后,得到标准状况下的氢气1.12L,则两种金属可能是
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室有黄铜(铜和锌两种金属的混合物)粉末。某兴趣小组欲利用给出的实验仪器及试剂,测定样品中锌的质量分数。除托盘天平必用外,供选择的实验装置如图所示;除样品黄铜外,供选择的药品有:足量的浓硫酸、足量的稀硫酸、足量氧化铜
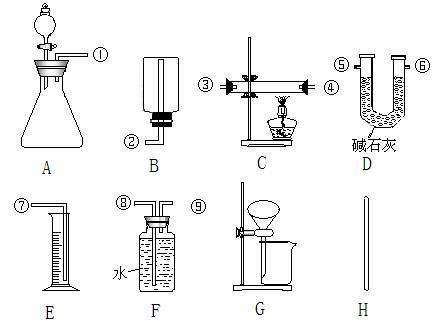
(1)你认为一定要用的药品是 。
(2)甲同学实验中使用了A、E、F三种装置,组装时接口编号的连接顺序为 。若实验过程中称得样品质量为a g,充分反应后生成的氢气体积为b L(标准状况下),则合金中锌的质量分数为 。
(3)乙同学称取黄铜的质量a g,充分反应后剩余固体的质量为d g。他在实验中使用了上图中 装置测定样品中锌的质量分数(填序号A…)。
(4)丙同学实验中只使用了A装置,他需要测得的实验数据有 和 。
(5)丁同学设计了另一种测定方法,他考虑使用A、C、D三种装置,并使用了足量的稀硫酸和氧化铜两种试剂,除称量黄铜的质量外,还称量了C装置反应前、后仪器和药品的质量,但他并不能准确测定出合金中锌的质量分数,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com