
某厂废水中含5.00×12-3mol·L-1的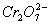 ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料 (
(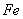 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:
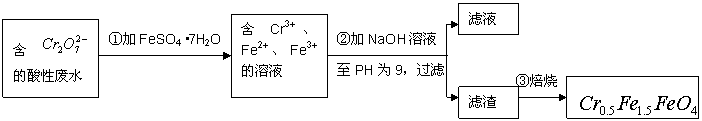
(1)第①步反应的离子方程式是
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有
(4)欲使1L该废水中的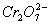 完全转化为
完全转化为 。理论上需要加入
。理论上需要加入
GFeSO4·7H2O。
【答案】
(1)Cr2O72- + 6Fe2+ + 14H+  2Cr3+ + 6Fe3+ + 7H2O
2Cr3+ + 6Fe3+ + 7H2O
(2)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照
(3)Fe(OH)3、Fe(OH)2
(4)13.9
【解析】(1)第①步是Cr2O72-与Fe2+发生氧化还原反应,方程式为:
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(2)测定溶液的pH的方法是:用玻璃棒蘸取待测溶液滴在pH试纸的中心位置,然后对照标准比色卡,读出对应颜色的数据;
(3)从最终所得磁性材料的化学式可知,滤渣中主要有Cr(OH)3、Fe(OH)2、Fe(OH)3;
(4)1L废水中的n(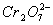 )=5.00×12-3mol,根据关系式:
)=5.00×12-3mol,根据关系式: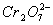 ~4Cr0.5Fe1.5FeO4~12FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol
~4Cr0.5Fe1.5FeO4~12FeSO4·7H2O,所以理论上n(FeSO4·7H2O)=0.05mol,m(FeSO4·7H2O)= 0.05mol
【考点分析】氧化还原反应综合应用


科目:高中化学 来源: 题型:
研究CO2的利用对促进低碳社会的构建具有重要的意义。
⑴已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为______________。
⑵高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是______________。
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图1,该电池反应的离子方程式为 ______________。


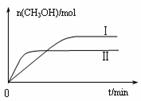
图1 图2 图3
⑶二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K=______________。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH_______(填“>” “<”或“=”)0。
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ________KⅡ(填“>” “<”或“=”)。
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物 投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学与生活的说法不正确的是 ( )
A.采用原煤脱硫技术,可减少燃煤产生的SO2
B.硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂
C.自来水厂可用氯气来杀菌消毒,因此氯气无毒
D.维生素C具有还原性,可用作食品抗氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A. 元素的单质一定由氧化或还原该元素的化合物制得
B. 含有最高价元素的化合物不一定具有很强的氧化性
C. 阳离子只能得到电子被还原,阴离子只能失去电子被氧化
D. 在化学反应中,得电子越多的氧化剂,其氧化性就越强
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是_______晶体,31g白磷与足量的氧气完全燃烧释放出745.5kJ的热量,请写出白磷燃烧的热化学反应方程式:_________________________________________;
(2)已知白磷和氯酸溶液可发生如下反应:
P4 + HClO3 + === HCl + H3PO4
配平并完成上述反应方程式,该反应的氧化剂是______________。
(3)白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:
12P4 + 60CuSO4 + 96H2O === 20Cu3P + 24 H3PO4 + 60 H2SO4
该反应的氧化产物是______________,若有1.1mol P4反应,则有________mol电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃、101 kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨,s)+O2(g)===CO2(g) ΔH=-393.51 kJ·mol-1①
C(金刚石,s)+O2(g)===CO2(g) ΔH=-395.41 kJ·mol-1②
据此判断,下列说法正确的是 ( )
A.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;石墨的能量比金刚石的高
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应:Co2O3 + 6HCl(浓) == 2CoCl2 + Cl2↑+ 3H2O (I)
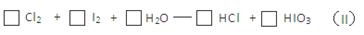
(1)反应(I)中的氧化剂是
(2)根据反应(I)计算,若生成标准状况下33.6L氯气时,电子转移数目是
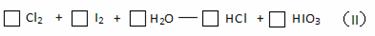 (3)将反应(II)配平
(3)将反应(II)配平
(4)反应(II) 中 发生氧化反应(5)HCl 、I2 、CoCl2三种物质的还原性由强到弱的顺序是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com