
下列指定反应的离子方程式正确的是
A.金属钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.用醋酸除去水垢中的碳酸钙:CaCO3+2H+ =Ca2++H2O+CO2↑
C.硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:2H++SO42-+Ba2++2OH-= 2H2O+BaSO4↓
D.电解饱和MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:填空题
【物质结构与性质】(15分)钙的化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔.请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为___________________.
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的π键数目为_________.
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N).丙烯腈分子中碳原子轨道杂化类型是_______________,构成丙烯腈元素中第一电离能最大的是__________.
(2)抗坏血酸钙的组成为Ca(C6H7O6)2?4H2O,其结构示意图如图1:

该物质中存在的化学键类型包括____________(填字母).
A.金属键 B.离子键 C.非极性共价键 D.配位键
(3)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图2所示:由此可判断该钙的氧化物的化学式为____________.已知阿伏加德罗常数为NA,该晶体的密度为ρg·cm3,则晶胞中两Ca2+间的最近距离为______________cm.(用含NA、ρ的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为1.0L的恒容密闭容器中,充入一定量的H2和SO2发生下列反应:
3H2(g)+SO2(g)  2H2O(g)+H2S(g)
2H2O(g)+H2S(g)
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
H2 | SO2 | H2 | SO2 | ||
容器I | 300 | 0.3 | 0.1 | / | 0.02 |
容器II | 300 | 0.6 | 0.2 | / | / |
容器III | 240 | 0.3 | 0.1 | / | 0.01 |
下列说法正确的是
A.该反应正反应为吸热反应
B.容器II达到平衡时SO2的转化率比容器I小
C.容器III达到平衡的时间比容器I短
D.240℃时,该反应的平衡常数为1.08×104L? mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:实验题
(15分)碘化钠是实验室中常见的分析试剂,常用于医疗和照相业。工业上通常用水合肼(N2H4·H2O,100℃以上分解)还原法制取碘化钠,工艺流程如下:
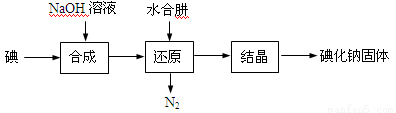
(1)合成过程的反应产物中含有IO3-,写出合成过程的离子方程式 。
(2)还原过程必须保持反应温度在60~70℃,这个温度既能保证反应的快速进行,又能 。工业上也可以用Na2S或Fe屑还原制备碘化钠,但水合肼还原法制得的产品纯度更高,原因是 。
(3)请补充完整检验还原液中是否含有IO3-的实验方案:取适量还原液, 。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液。
(4)测定产品中NaI含量的实验步骤如下:
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中;
c.用0.1000mol·L-1AgNO3溶液滴定至终点,记录消耗AgNO3溶液的体积;
d.重复b、c操作2~3次,记录相关实验数据。
①滴定过程中,AgNO3溶液应放在 中;步骤d的目的是 。
②若用上述方法测定产品中的NaI含量偏低(忽略测定过程中的误差),其可能的原因是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:选择题
化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得
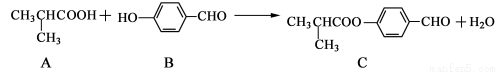
下列说法正确的是
A.每个A分子中含有1个手性碳原子
B.可以用酸性KMnO4溶液检验B中是否含有醛基
C.1molC分子最多可与4molH2发生加成反应
D.C可发生加成反应、取代反应、氧化反应、消去反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:选择题
下列有关化学用语的表示正确的是
A.NH4Cl的电子式: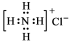 B.Cl-的结构示意图:
B.Cl-的结构示意图:
C.中子数为21的钾原子:40 19K D.对硝基苯酚的结构简式: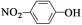
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏常州市高三第一次调研试卷化学试卷(解析版) 题型:实验题
(12分)某兴趣小组的同学发现,将CuSO4溶液与Na2CO3溶液混合会产生蓝绿色沉淀。他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究。
【提出猜想】
猜想1:所得沉淀为 ;
猜想2:所得沉淀为 ;
猜想3:所得沉淀为碱式碳酸铜[化学式可表示为mCu (OH)2·nCuCO3]。
查阅资料获知,无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干。
步骤2:取一定量所得固体,用如下装置(夹持仪器未画出)进行定性实验。
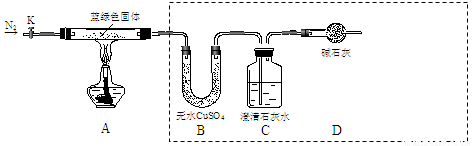
能证明猜想1成立的实验现象是 。
【问题讨论】
(1)检查上述虚线框内装置气密性的实验操作是:关闭K, 。
(2)若在上述装置B中盛放无水CaCl2,C中盛放Ba(OH)2溶液,还可测定所得沉淀的组成。
①C中盛放Ba(OH)2溶液,而不使用澄清石灰水的原因是 。
②若所取蓝绿色固体质量为27.1 g,实验结束后,装置B的质量增加2.7 g,C中产生沉淀的质量为19.7 g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省肇庆市高三第一学期期末考试化学试卷(解析版) 题型:实验题
(16分)利用某地的闪锌矿(主要成分为ZnS,其杂质主要为铁、铜元素等)冶炼纯锌的传统工艺如下:

注:锌、铁、铜的沸点依次为1180K、2862K、1800K
(1)高温焙烧时,若氧气足量,则ZnS发生的化学反应方程式为 。
(2)方案1由锌熔体获得粗锌的的操作为 (填:“蒸馏”、“分馏”或“干馏”)。
(3)工业生产中方案2中固相2的成分为 ,液相1所含金属阳离子为:
(4)方案2中从液相1获取粗锌的过程中可用加入单质 除掉其他杂质;对比两种方案,方案2的优点是 。
(5)方案2的系列操作产生的废液可以制取绿矾。硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示:
温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 70 | 80 | 90 |
溶解度 | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 33.5 |
析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | ||||||
从上表数据可以得出的结论是:① ;② 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市昌平区高二上学期期末考试化学试卷(解析版) 题型:选择题
某有机物P中碳和氢原子个数比为3∶4,不能与溴水反应却能使酸性KMnO4溶液褪色。其蒸气密度是相同状况下甲烷密度的7.5倍。在铁存在时与溴反应,能生成2种一溴代物。以下说法正确的是
A.P属于烃的衍生物
B.P可以发生加成反应但不能发生取代反应
C.P中含苯环且有可能两个对位取代基
D.P在光照条件下与溴反应,可以生成3种溴代物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com