
| A、2 | B、3 | C、4 | D、5 |
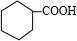 ,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代.
,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代. ,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代,故其环上的一氯代物有4种,故选C.
,环上的取代物,除了-COOH的邻、间、对位置外,羧基连接的碳也还有氢原子,可以取代,故其环上的一氯代物有4种,故选C.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| A、K+、NO3-、OH-、Cl- |
| B、SO42-、Mg2+、Cl-、Na+ |
| C、SO42-、Na+、Mg2+、CH3COO- |
| D、Cl-、SCN-、K+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,使用pH计测定浓度均为0.1mol/L NaClO、CH3COONa的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 | 检验蔗糖水解产物具有还原性 |
| C | 向新生成的AgCl悬浊液中滴入KI溶液 | 研究沉淀的转化 |
| D | 室温下,向两支装有同体积同浓度过氧化氢溶液的试管中,分别加入3滴同浓度的氯化铜、氯化铁溶液 | 研究催化剂对反应速率的影响 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入铝粉生成H2的溶液中,K+、Cu2+、SO42-、ClO-能大量共存 |
| B、在c(OH-)=10-2 mol?L-1的溶液中,NO3-、Ba2+、Cl-、Br-能大量共存 |
| C、0.1 mol/L Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| D、0.1 mol/L Na2CO3溶液中:2c(Na+)=c(H2CO3)+c(CO32-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、X、Y元素的金属性 X<Y |
| B、X、Y、Z、W的单质都具有可燃性 |
| C、Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D、一定条件下,W单质可以与Z的氢化物反应生成ZW |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH=6的H2SO4 稀释1000倍后,c(H+)=2c(SO42-) |
| B、0.1mol?L-1的Na2CO3溶液中:c(OH- )=c(HCO3- )+c(H+)+c(H2CO3) |
| C、浓度均为0.1mol?L-1的NaClO溶液和CH3COONa溶液中,c(ClO-)<c(CH3COO-) |
| D、浓度分别为0.1mol?L-1和0.01mol?L-1的CH3COOH溶液中:c(CH3COO-)前者是后者的10倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com