
| A. | 相等 | B. | ②多 | C. | ①多 | D. | 无法判断 |
分析 两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑、H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而①中氢气还原CuO,应先通入氢气排出装置中的空气,不能全部参与还原反应.
解答 解:两方案中所发生的化学方程式为:①Fe+H2SO4═FeSO4+H2↑、H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
②CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于部分氢气被浪费,从而导致铁的质量被多消耗一部分,所以导致方案①对应的铜减少.故方案②生成的铜多,
故选B.
点评 本题考查制备物质方案,为高频考点,把握制备中发生的反应、分析方案的差别为解答的关键,注意氢气还原氧化铜的实际操作即可解答,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
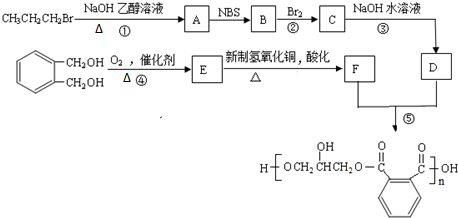

 .
. .
.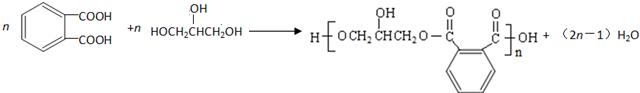 .
.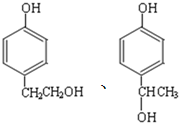 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+ | B. | Cl- | C. | Mg2+ | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com