
把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3 mol NO2和0.2 mol NO。向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止。得到固体质量不可能为
A.18 g  B.24 g C.30 g D.36 g
B.24 g C.30 g D.36 g
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
根据下列化学反应和事实,说明反应利用了硫酸的什么性质,将表示性质的选项的字母填在各小题的横线上。
A.不挥发性 B.酸性
C.吸水性 D.脱水性
E.强氧化性 F.强酸性
(1)浓硫酸可作气体干燥剂________;
(2)蔗糖中加浓H2SO4产生“黑面包”现象________;
(3)2NaCl+H2SO4(浓)Na2SO4+2HCl↑________;
(4)Zn+H2SO4(稀)===ZnSO4+H2↑________;
(5)Na2SO3+H2SO4(稀)===Na2SO4+SO2↑+H2O________;
(6)Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O________;
(7)C+2H2SO4(浓)2SO2↑+2H2O+CO2↑________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业常用燃料与水蒸气反应制备H2和CO, 再用H2和CO合成甲醇。
(1)制取H2和CO通常采用:C(s)+H2O(g)  CO(g)+H2(g) △H=+131.4 kJ·mol-1,下列判断正确的是 。
CO(g)+H2(g) △H=+131.4 kJ·mol-1,下列判断正确的是 。
a.该反应的反应物总能量小于生成物总能量
b.标准状况下,上述反应生成1L H2气体时吸收131.4 kJ的热量
c.若CO(g)+H2(g) C(s)+H2O(1) △H=-QkJ·mol-1,则Q<131.4
C(s)+H2O(1) △H=-QkJ·mol-1,则Q<131.4
d.若C(s)+CO2(g) 2CO(g) △H1;CO(g)+H2O(g)
2CO(g) △H1;CO(g)+H2O(g) H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO,该反应为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
已知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
| 不同时间各物质的物质的量/mol | ||||
| 0 min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |
根据表中数据计算:
①0 min ~ 2min 内H2的平均反应速率为 。
②达平衡时, CH4的转化率为 。在上述平衡体系中再充入2.00mol甲烷和1.00mol 水蒸气,达到新平衡时H2的体积分数与原平衡相比 (填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有______。(填字母)
a.CO的含量保持不变 b.容器中c(CH4)与c(CO)相等
c.容器中混合气体的密度保持不变 d.3ν正(CH4)=ν逆(H2)
(3)合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图( c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。
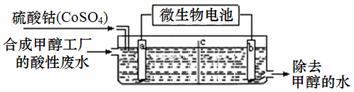
①a电极的名称为 。
②写出除去甲醇的离子方程式 。
③微生物电池是绿色酸性燃料电池,写出该电池正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废气中氮的氧化物是重要的污染源,有一种治理污染的方法是通入适量氨气将其还原为无毒物质N2和H2O,现有含氮氧化物NO和NO2的混合气体3L,用相同条件下的NH3 3L恰好反应完全,则混合气中NO与NO2的体积分数比
A.l:4 B.1:3 C .l:2 D.l:l
.l:2 D.l:l
查看答案和解析>>
科目:高中化学 来源: 题型:
A是一取代芳香化合物,相对分子质量为136,分子中只含碳、氢、氧,其中氧的含量为23.5%。实验表明: A的芳环侧链上只含一个官能团;A和NaOH溶液反应后酸化可以得到E(C7H6O2)和F。
(1)A、E、F的结构简式。
(2)A和NaOH溶液反应、酸化的实验装置如下:
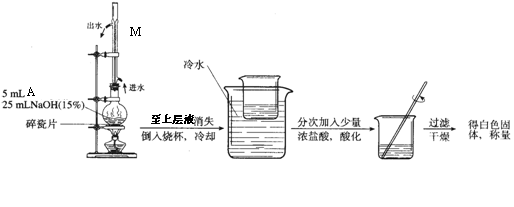

写出A与NaOH溶液反应的化学反应方程式 。
写出实验装置中M的名称和作用 。
(3)A有多种同分异构体,符合下列条件的结构共有 种,
①可以发生银镜反应 ②属于芳香族化合物,不具备其它环状结构
③可以与氢氧化钠溶液反应 ④不能与FeCl3发生显色反应
请写出其中核磁共振氢谱有5个吸收峰的A的结构的结构简式:
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组设计了如下实验装置,欲探究铜和浓硝酸的反应是否有一氧化氮产生,如果有,什么浓度的硝酸就会产生NO(假设硝酸和铜的反应产物只可能产生NO或NO2 ,题中所涉气体体积均为标准状况下的数据,且忽略反应中溶液体积的变化)。

试回答下列问题:
(1)C装置中将铜粉分散在石棉绒中的原因是:______________________________;
B装置的作用为_______________________________________。
(2)在铜和浓硝酸反应前,挤压打气球鼓入空气,经A、B、C反应后,进人D中的气体主要是(填化学式),通入该气体的目的是______________________________;进行此步操作时应关闭,打开______(填k1,k2或k3)。
(3)关闭k1,k2,打开k3 ,由分液漏斗向装有一定量铜片的D中滴加14 mol/L浓硝酸10. 00 mL。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。你认为这么操作的目的是______________。
(4)若E中出现倒吸,可采取的应急操作是____________________________。
(5)从E装置所得溶液中取出25. 00 mL,加2-3滴酚酞试液,用0. 1000 mol/L的NaOH溶液滴定,当滴定达到终点时消耗NaOH溶液50. 00 mL;若实验结束后冷却到常温,准确测得F装置实验前后量气管的读数差值为386. 00 mL。从上述所得数据进行计算、分析,试判断_____________(“能”或“不能”)完成实验的探究目的;上述铜与浓硝酸反应中铜片____________(填‘过足”、“不足”或“恰好”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
中央电视台曾报道纪联华超市在售的某品牌鸡蛋为“橡皮弹”, 煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋。专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致。其结构简式如右图所示:下列说法不正确的是
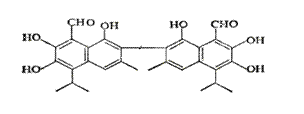
A、该化合物的分子式为:C30H30O8
B、1mol棉酚最多可与10mol H2加成,与6molNaOH反应
C、在一定条件下,可与乙酸反应生成酯类物质
D、该物质可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.含金属元素的离子一定是阳离子
B.应用蒸馏的方法,可以分离沸点相差较大的液体混合物
C.氯水和过氧化钠都具有漂白作用,其漂白原理相似
D.高炉炼铁时,还原铁矿石的还原剂为一氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com