
某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去)。

(1)装置B中发生反应的化学方程式是 。
(2)虚线框图C的气体收集装置是下图中的 (选填字母编号)。

(3)反应停止,待B管冷却后,称量,得到固体质量为28.8g。再向固体中加入过量稀盐酸充分反应,并进行如下实验:

试剂a的化学式是 ,试剂b的化学式是 ;加入新制氯水后溶液红色加深的原因是(用离子方程式表示) 。
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现请对褪色原因进行探究。首先提出假设。假设1:溶液中的+3价铁被氧化为更高的价态;假设2:
;为了对所提出的假设2进行验证,实验方案是
。
(5)根据所给数据,可计算出反应后B装置中铁元素的质量分数为 。
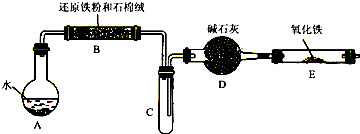
(1)3Fe + 4H2O 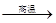 Fe3O4
+ 4H2↑ (1分)
Fe3O4
+ 4H2↑ (1分)
(2)bd (2分)
(3)KSCN ,NaOH;2Fe2++Cl2→2Fe3++2Cl- (1分1格,共3分)
(4)SCN-被过量的氯水氧化;(2分)
取少量褪色后的溶液,滴加过量KSCN溶液,如果出现红色,则说明假设2 正确,若不变红,则假设2不正确。(2分)
(5)77.8% (2分)
【解析】
试题分析:(2)氢气难溶于水,可用排水法收集。选bd。
(3)因为铁和水反应生成Fe3O4,Fe3O4,+8HCl=2FeCl3+FeCl2+4 H2O 。淡黄色溶液含少量Fe3+,加a:KSCN,Fe3++3SCN- =Fe(SCN)3 少量淡红色。加新制的氯水,把FeCl2氧化变成FeCl3和KSCN生成
Fe(SCN)3,再加NaOH,能生成Fe(OH)3 。加热Fe(OH)3变成红棕色的Fe2O3
(4)“SCN-被过量的氯水氧化”,为证明此假设,需加过量的KSCN溶液,看是否变红。
(5)解设原铁元素的质量为x
2Fe------- Fe2O3
2*56 160
x 32 x=22.4
Fe%=22.4*100%/28.8=77.8%
考点:本题以化学实验为基础,考查实验设计、实验操作、分析和化学计算等知识。


科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入适量盐酸,微热 | 黑色粉末全部溶解,溶液呈 浅绿色 浅绿色 ,有少量气泡产生 |
| Ⅱ | 向实验Ⅰ中得到的溶液加几滴KSCN溶液,振荡 | 溶液不显血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
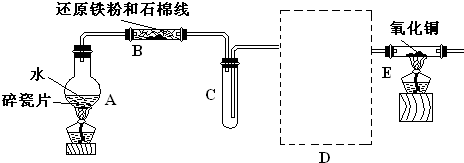
 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验.(图中夹持及尾气处理装置均已略去)
某校化学小组学生利用如图所列装置进行“铁与水反应”的实验.(图中夹持及尾气处理装置均已略去)
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
新型材料纳米![]() 粉具有超强的磁性能,可用作高密度磁记录的介质以及高效催化剂等。在不同温度下,
粉具有超强的磁性能,可用作高密度磁记录的介质以及高效催化剂等。在不同温度下,![]() 粉与水蒸气反应的固体产物不同:温度低于570℃时,生成FeO,高于570℃时,生成Fe3O4。某校化学小组学生利用下图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去)。
粉与水蒸气反应的固体产物不同:温度低于570℃时,生成FeO,高于570℃时,生成Fe3O4。某校化学小组学生利用下图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去)。
 |
(1)在高温下,装置B中发生反应的化学方程式是 。
(2)请在下列装置中选择满足虚线框图C的气体收集装置 。
 |
(3)该小组同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
【查阅资料】该小组同学通过资料得知,固体产物中一般不会同时出现三种形态混合物组合。
【提出假设】
假设1:全部为氧化亚铁;
假设2:全部为四氧化三铁;
假设3:铁和氧化亚铁混合物;
假设4:铁和四氧化三儿混合物;
假设5: 。
【设计方案】小组成员讨论后对假设4提出实验方案(不要在答题卡上作答)
【实验过程】
根据上述设计的方案进行实验。在答题卡上按下表的格式写出实验步骤、预期现象与结论。
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入适量盐酸,微热 | 黑色粉末全部溶解,溶液呈 ,有少量气泡产生 |
| Ⅱ | 向实验Ⅰ中得到的溶液加几滴KSCN溶液,振荡 | 溶液不显血红色 |
【交流讨论】①实验步骤Ⅱ加入 KSCN后溶液不显血红色的原因 。
②继续向Ⅱ溶液中加稀硝酸,立即出现血色,写出该过程中发生变化的
离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com