
�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
�� CH3OH(g)+H2O(g)=CO2(g)+3H2(g)����H=��49.0 kJ/mol
�� CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)����H=��192.9 kJ/mol
����˵����ȷ����
| A��CH3OH��ȼ��Ϊ���ȷ�Ӧ |
B����Ӧ���е������仯��ͼ��ʾ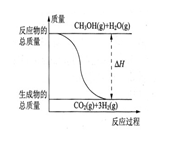 |
| C��CH3OHת���H2�Ĺ���һ��Ҫ�������� |
| D�����ݢ���֪��Ӧ��CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)�ġ�H >��192.9kJ/mol |
D
�������������ȼ�ն��Ƿ��ȷ�Ӧ����CH3OH��ȼ��Ϊ���ȷ�Ӧ��ѡ��A����ȷ����Ӧ�������ȷ�Ӧ����Ӧ����������������������������ѡ��B����ȷ����Ӧ����Ҳ���������ɣ�����Ӧ�Ƿ��ȷ�Ӧ������ѡ��C����ȷ����̬�״�����������Һ̬�״�������������Һ̬�״�������Ӧ�ڷų��������٣�����Խ�٣���HԽС��ѡ��D��ȷ����ѡD��
���㣺���鷴Ӧ�ȵ��й��жϺͼ���
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������߿����������У�����������ѧ���������������ͷ�ɢ˼ά��������ȷӰ�췴Ӧ�ȵĴ�С�����ǽ���Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���й��ڻ�ѧ��Ӧ����������ȷ����
| A����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ |
| B����֪NaOH(aq) +HCI(aq) =NaCI(aq)+H2O��1�� ��H= һ57��3 kJ��mol-1�� ��40��0 g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�57��3 kJ������ |
| C��CO(g)��ȼ������283��0 kJ��mol-1�����ʾCO(g)��ȼ���ȵ��Ȼ�ѧ����ʽΪ 2CO (g)+ O2(g)=2CO2(g) ��H=һ283��0 kJ��mol-1 |
| D����֪2C(s) +2O2(g)=2CO2(g) ��H=a, 2C(s) +O2(g)="2CO" (g) ��H=b����b>a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ѧ�������ܡ����ܵ����ת�������ڻ�ѧ�������������ת����˵����ȷ����
| A����ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ��������� |
| B�����ȷ�Ӧ��, ��Ӧ�������������������������� |
| C��ͼI��ʾ��װ���ܽ���ѧ��ת��Ϊ���� |
| D��ͼII��ʾ�ķ�ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����2��5��̼ԭ�ӵ�ֱ�������е��ȼ���ȵ����ݼ��±���
| �������� | ���� | ���� | ���� | ���� |
| �е�/�� | ��88.6 | ��42.1 | ��0.5 | 36.1 |
| *ȼ����/kJ��mol��1 | 1 560.7 | 2 219.2 | 2 877.6 | 3 535.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
36g̼����ȫȼ�����������У�COռ����֮һ�����CO2ռ����֮���������֪��2C(s)+O2(g)=2CO(g)��H=-110.5kJ/mol,2CO(g)+O2(g) =2CO2(g)��H=-566kJ/mol,����Щ̼��ȫȼ����ȣ���ʧ�������ǣ� ��
| A��172.5kJ | B��1149kJ | C��517.5kJ | D��283kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ������������з���δ������Դ�����ǣ� ��
����Ȼ�� ��ú ��ʯ�� ��̫���� ���������� ���� ������
| A���٢ڢۢ� | B���ۢݢޢ� | C���ܢݢޢ� | D���ۢܢݢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��9�֣���1����(N2H4)�ֳ��������ڳ�������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϡ���֪��101kPaʱ��1gN2H4����������ȫȼ�����ɵ�����H2O���ų�19.5kJ����(25��ʱ)����ʾN2H4ȼ���ȵ��Ȼ�ѧ����ʽ��____________________________________________________��
��2���£�����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ���£�����ȼ�ϵ�طŵ�ʱ�������ĵ缫��Ӧʽ��__________________�������ĵ缫��Ӧʽ��_______________��
��3����ͼ��һ��������ʾ��ͼ��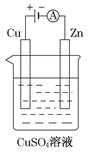
��пƬ�Ϸ����ĵ缫��Ӧʽ�ǣ�_____________________________��
�ڼ���ʹ���£�����ȼ�ϵ����Ϊ�ù����еĵ�Դ��ͭƬ�����仯Ϊ128g�����£�����ȼ�ϵ�����������ı�״���µĿ���________L(��������������������Ϊ20%)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��5�֣�ijʵ��С��ͬѧ��������ʵ�飬��̽����ѧ��Ӧ�е������仯��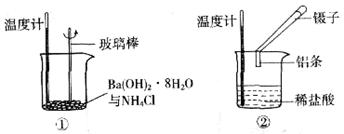
��1��ʵ����������е��¶Ƚ��ͣ��ɴ��ж����������������Ȼ�茶��巴Ӧ��____________������ȡ����ȡ�����Ӧ��
��2��ʵ����У���С��ͬѧ���ձ��м���5 mL 1.0 mol/L���ᣬ�ٷ�����ɰֽ��ĥ�����������۲����H2�����ʣ���ͼA��ʾ���÷�Ӧ��____________������ȡ����ȡ�����Ӧ���������仯������ͼ�е�____________���B����C������ʾ��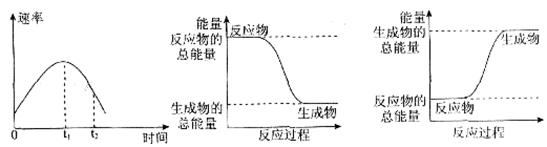
ͼA��0һtl�λ�ѧ��Ӧ���ʱ仯��ԭ����_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ſ�ѧ�����Ľ��������������˶��ּ״����ӽ���Ĥȼ�ϵ�أ������㲻ͬ������
��1����һ��״����ӽ���Ĥȼ�ϵ�أ��轫�״�����ת��Ϊ���������ַ�Ӧԭ����
A��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ��H����49.0kJ/mol
B��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H����192.9kJ/mol
��֪H2O(l)��H2O(g) ��H����44 kJ/mol����д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ ��
��2����ͼ��ij�ʼDZ������ü״����ӽ���Ĥȼ�ϵ�صĽṹʾ��ͼ���״��ڴ����������ṩ���Ӻ͵��ӣ����Ӿ����·�����Ӿ��ڵ�·������һ����������Ӧ������ܷ�ӦΪ��2CH3OH��3O2��2CO2��4H2O����c�缫�� �������������������
c�缫�Ϸ����ĵ缫��Ӧʽ�� ��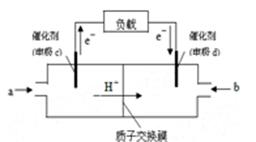
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com