
多硫化钠Na2Sx(x≥2)在结构上与Na2O2、FeS2、CaC2等有相似之处.Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值是( )
|
| A. | 5 | B. | 4 | C. | 3 | D. | 2 |
| 化学方程式的有关计算;氧化还原反应.. | |
| 专题: | 压轴题;计算题;氧化还原反应专题. |
| 分析: | Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,S元素化合价由﹣升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:16,根据电子转移守恒,列方程计算x的值. |
| 解答: | 解:Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,S元素化合价由﹣升高为+6,而NaClO被还原为NaCl,Cl元素化合价由+1价降低为﹣1价,反应中Na2Sx与NaClO的物质的量之比为1:16,根据电子转移守恒,则: x×[6﹣(﹣)]=16×[1﹣(﹣1)] 解得:x=5 故选A. |
| 点评: | 本题考查氧化还原反应的计算,难度中等,注意平均化合价的利用与氧化还原反应中守恒思想的运用. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
有机物分子式为C5H12O2,0.1 mol该有机物与足量钠反应产生的气体在标准状况下的体积为2.24 L,则它含有两个甲基的稳定结构(不考虑立体异构,不考虑同一个碳原子上连接两个相同官能团的结构)有( )。
A.6种 B.7种 C.8种 D.9种
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活、环境等关系密切,下列有关说法正确的是
A.铜属于重金属,但其盐有毒,所以铜质器皿不安全,应该禁用
B.食盐、食醋和味精是常用的食品添加剂,其主学成分均属钠盐
C.氨气液化以及液氨气化均要吸收大量的热,所以氨常用于制冷剂
D.SO2能使食物增白,但这类食物会严重损害人体的肝肾,所以食品中应该严格限量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是: (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填代号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)
①由滤液B制备氯化铝晶体(将AlCl3•6H2O)涉及的操作为: 、冷却结晶、 (填操作名称)、洗涤。
②将AlCl3•6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的 (填序号).
①氧化性 ②吸水性 ③难挥发性 ④脱水性
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。
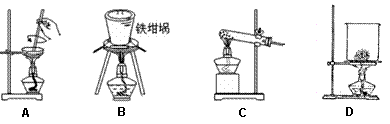
查看答案和解析>>
科目:高中化学 来源: 题型:
大量事实证明,水溶液中并不存在H+、AlO2﹣等离子,实际存在的是H30+、[Al(OH)4]﹣.铝和强碱溶液的反应可以理解为铝在碱性环境下先与水反应,而后进一步与强碱反应(反应均不可逆).对于Al与重氢氧化钠(NaOD)的水溶液反应(假定水中不含氘和氚),下列说法正确的是( )
|
| A. | 生成的氢气中只含有D2 | B. | 生成的氢气中只含有H2 |
|
| C. | 生成的氢气中含有H2、HD、D2 | D. | 以上判断都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
①液体量不超过烧瓶容积,不少于.
②温度计的水银球应位于蒸馏烧瓶支管口附近.
③为防止暴沸,应在烧瓶中加入沸石或碎瓷片.
④冷凝管中冷却水下进上出,先加热,再通水.
⑤按各组分沸点控制分馏温度,并收集在同一锥形瓶中
⑥停止加热后,应继续通水冷却冷凝管中蒸气.
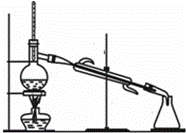
|
| A. | ①③④ | B. | ②③④ | C. | ③④⑤ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO (aq)PbCO3(s)+SO
(aq)PbCO3(s)+SO (aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K=____________________________________。
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在________溶液中PbSO 4转化率较大,理由是___________________________。
4转化率较大,理由是___________________________。
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],它和PbCO3受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO4)的成分提出如下假设,请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:_____________________________________________________________;
假设三:____________________________________ _________________________。
_________________________。
(4)为验证假设一是否成立,课题组进行如下研究。
①定性研究:请你完成下表中内容。
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥,…… |
②定量研究:取26.7 mg的干燥样品,加热,测得固体质量随温度的变化关系如下图:

某同学由图中信息得出结论:假设一不成立。你是否同意该同学的结论,并简述理由:
__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽 草酸的说法正确的是
草酸的说法正确的是
 A.分子式为C7H6O5
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
风靡全球的饮料果醋中含有苹果酸(MLA),其分子式为C4H6O5。0.1 mol苹果酸与足量NaHCO3溶
液反应能产生4.48 L CO2(标准状况),苹果酸脱水能生成使溴水褪色的产物。如图表示合成MLA的路线。
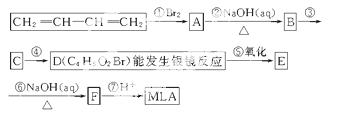
(1)写出下列物质的结构简式:A________,D________。
(2)指出反应类型:①________,②________。
(3)写出所有与MLA具有相同官能团的同分异构体的结构简式:
___________________________________________________________________
__________________________________ __________________________________。
__________________________________。
(4)写出E—→F转化的化学方程式________________________________________。
(5)MLA可通过下列反应合成一高分子化合物G[(C6H8O4)n],
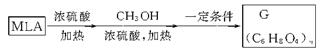 则G的结构简式为_________。
则G的结构简式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com