
| A£® | ČŻĘ÷ÖŠ·¢ÉśµÄ·“Ó¦æɱķŹ¾ĪŖ3X£Øg£©+Y£Øg£©ØT2Z£Øg£© | |
| B£® | ·“Ó¦½ųŠŠµÄĒ°3 minÄŚ£¬ÓĆX±ķŹ¾µÄ·“Ó¦ĖŁĀŹv£ØX£©=0.2 mol/£ØL•min£© | |
| C£® | ±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżK¼õŠ” | |
| D£® | Čōøı䷓ӦĢõ¼ž£¬Ź¹·“Ó¦½ų³ĢČēĶ¼3ĖłŹ¾£¬ŌņøıäµÄĢõ¼žŹĒŌö“óŃ¹Ēæ |
·ÖĪö A”¢øł¾ŻĪļÖŹµÄĮæµÄ±ä»ÆĮæÓė»Æѧ¼ĘĮæŹż³ÉÕż±ČŹéŠ“»Æѧ·½³ĢŹ½£»
B”¢øł¾Ż3minÄŚXµÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆĮæ¼ĘĖć»Æѧ·“Ó¦ĖŁĀŹ£¬v=$\frac{”÷c}{”÷t}$£»
C”¢øł¾ŻĶ¼2ÖŠĒśĻߵĊ±ĀŹ“óŠ”ÅŠ¶ĻĪĀ¶ČµÄøßµĶ£¬ĻČ¹ÕĻČĘ½ĪĀ¶Čøߣ¬½įŗĻ»ÆŃ§Ę½ŗāŅʶÆŌĄķÅŠ¶ĻŅĘ¶Æ·½Ļņ£»
D”¢Ķ¼3ÓėĶ¼1±Č½Ļ£¬“ļµ½Ę½ŗāµÄŹ±¼äĖõ¶Ģ£¬Ę½ŗāדĢ¬ĪļÖŹµÄĮæ²»±ä£¬ÅŠ¶ĻĘ½ŗā²»·¢ÉśŅĘ¶Æ£¬øł¾ŻÓ°ĻģĘ½ŗāŅĘ¶ÆµÄŅņĖŲÅŠ¶Ļ£®
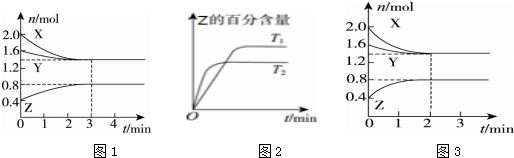
½ā“š ½ā£ŗA”¢øł¾ŻĶ¼1·ÖĪö£¬·“Ó¦ÖŠX”¢YµÄĪļÖŹµÄĮæÖš½„¼õŠ”£¬ZµÄĪļÖŹµÄĮæÖš½„Ōö“ó£¬ĖłŅŌX”¢YĪŖ·“Ó¦Īļ£¬ZĪŖÉś³ÉĪļ£¬ÓÉÓŚøĆ·“Ó¦·“Ó¦ĪļƻӊĶźČ«·“Ó¦£¬øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬øł¾ŻĪļÖŹµÄĮæµÄ±ä»ÆĮæÓė»Æѧ¼ĘĮæŹż³ÉÕż±ČæÉÖŖ0.6mol£ŗ0.2mol£ŗ0.4mol=3£ŗ1£ŗ2£¬ĖłŅŌ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3X£Øg£©+Y£Øg£©?2Z£Øg£©£¬¹ŹA“ķĪó£»
B”¢·“Ó¦½ųŠŠµÄĒ°3minÄŚ£¬v£ØX£©=$\frac{0.6mol}{2L”Į3min}$=0.1mol/£ØL•min£©£¬¹ŹB“ķĪó£»
C”¢øł¾ŻĶ¼2ÖŠĒśĻߵĊ±ĀŹ“óŠ”ÅŠ¶Ļ£¬T2Ź±Ļȵ½“ļĘ½ŗāדĢ¬£¬ĖµĆ÷·“Ó¦ĖŁĀŹ“ó£¬øł¾ŻĪĀ¶ČŌ½øß·“Ó¦ĖŁĀŹŌ½“óĖµĆ÷T2ĪĀ¶Čøߣ¬ĪĀ¶ČÉżøߏ±ZµÄ°Ł·Öŗ¬Įæ½µµĶ£¬ĖµĆ÷ÉżĪĀĘ½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ŌņĘ½ŗā³£Źż¼õŠ”£¬¹ŹCÕżČ·£»
D”¢Ķ¼3ÓėĶ¼1±Č½Ļ£¬Ķ¼3µ½“ļĘ½ŗāĖłÓƵď±¼ä½Ļ¶Ģ£¬ĖµĆ÷·“Ó¦ĖŁĀŹŌö“󣬵«Ę½ŗāדĢ¬Ć»ÓŠ·¢Éśøı䣬ӦŹĒ¼ÓČė“߻ƼĮĖłÖĀ£¬ČōŹĒŃ¹ĒæŌö“óĘ½ŗāÕżĻņ½ųŠŠ£¬Ę½ŗāדĢ¬øı䣬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāŅʶÆŅŌ¼°Ę½ŗāĶ¼ĻóĢā£¬×öĢāŹ±×¢Ņā·ÖĪöĶ¼ĻóÖŠĒśĻߵıä»Æ¹ęĀÉ£¬½įŗĻĶā½ēĢõ¼ž¶ŌĘ½ŗāŅĘ¶ÆµÄÓ°Ļģ½ųŠŠ·ÖĪö£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×ÓŹ½ŹĒC3H8O3 | |
| B£® | A“ß»ÆŃõ»ÆµÄ²śĪļÄÜ·¢ÉśŅų¾µ·“Ó¦ | |
| C£® | 0.1molAÓė×ćĮæNa·“Ó¦Äܹ»²śÉś2.24LH2£Ø±ź×¼×“æö£© | |
| D£® | AŌŚŅ»¶ØĢõ¼žĻĀÄÜ·¢Éś¼Ó¾Ū·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 300mL0.1mol•L-1Na2SO4ČÜŅŗÖŠNa+ÅضČĪŖ0.6mol•L-1 | |
| B£® | ±ź×¼×“æöĻĀ£¬22.4LH2OĖłŗ¬Ō×ÓŹżĪŖ3NA | |
| C£® | 1molH3O+ÖŠĖłŗ¬ÓŠµē×ÓŹżĪŖ10NA | |
| D£® | 0.2mol•L-1Ba£ØNO3£©2ČÜŅŗÖŠNO${\;}_{3}^{-}$Ąė×ÓŹżĪŖ0.4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«58.5 g NaClČÜÓŚ1 LĖ®ÖŠæɵĆ1 mol•L-1µÄNaClČÜŅŗ | |
| B£® | “Ó1 L 1 mol/LµÄNaClČÜŅŗÖŠČ”³ö10 mL£¬ĘäÅضČČŌŹĒ1 mol/L | |
| C£® | ÖŠŗĶ100 mL 1 mol/LµÄH2SO4ČÜŅŗÉś³ÉÕżŃĪ£¬ŠčNaOH 4 g | |
| D£® | ½«78 g Na2O2ČÜÓŚĖ®£¬Åä³É1 LČÜŅŗæɵƵ½ÅضČĪŖ1 mol•L-1ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż”¢Äę·“Ó¦²»ŌŁ½ųŠŠ | B£® | ÅضČĪŖĮć | ||
| C£® | Õż”¢Äę·“Ó¦¶¼»¹ŌŚ¼ĢŠų½ųŠŠ | D£® | Õż”¢Äę·“Ó¦µÄĖŁĀŹĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮ·ŪÓėŃõ»ÆĆ¾¹²ČČæÉÖĘČ”½šŹōĆ¾ | |
| B£® | ĀĮ·Ö±šÓė×ćĮæµÄ HClČÜŅŗ”¢×ćĮæµÄNaOHµÄČÜŅŗ·“Ó¦£¬²śÉśµÄĒāĘųĒ°Õ߶ą | |
| C£® | ĀČ»Æ¹Æ£ØHgCl2£©µÄĻ”ČÜŅŗæÉÓĆÓŚŹÖŹõĘ÷ŠµĻū¶¾£¬ŅņĪŖĖü»įŹ¹µ°°×ÖŹ±äŠŌ£¬É±¾śĻū¶¾ | |
| D£® | NaOHČÜŅŗæÉŅŌŹ¢×°ŌŚ“ų²£Į§ČūµÄÄ„æŚŹŌ¼ĮĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8øöÖŠ×ÓµÄĢ¼Ō×ÓµÄŗĖĖŲ·ūŗÅ£ŗ12C | B£® | HFµÄµē×ÓŹ½£ŗ | ||
| C£® | ĀČ»ÆĆ¾  | D£® | Cl-Ąė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com