
����Ŀ���ҹ�����ʹ�õ�ʳ�ο����Ŀǰ�У������軯�ء�����ơ��������������ά�ء��������涨ʳ���������軯[K4Fe(CN)6]�����ʹ����Ϊ10mgkg��1��
��1����̬��ԭ�Ӻ���������ߵĵ��������ܼ��Ĺ����ĿΪ__________��K4Fe(CN)6��Fe2+����Χ�����Ų�ͼΪ_________________��
��2��K4Fe(CN)6�д���_____________������ţ���
A�����Ӽ� B���Ǽ��Լ� C����λ�� D������ E������
��3��д����CN-��Ϊ�ȵ���������ӵĵ���ʽΪ______________________
��4���������������Ŀռ乹��Ϊ______________���������辧���й�ԭ�ӵ��ӻ���ʽΪ_____
��5�������軯����Һ��ϡ�������ʱ������������ԭ��Ӧ�����������κ�һ����CN���ǵȵ��������̬�������Ӧ��ѧ����ʽΪ_______________��
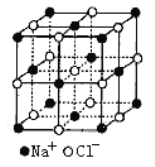
��6��FeO����ľ�����NaCl�����ƣ�NaCl�ľ�����ͼ��ʾ�����ھ���ȱ�ݣ�ij�������������ʵ�����ΪFe0.9O�����а�����Fe2+��Fe3+�������߳�Ϊ428pm����þ�����ܶ�Ϊ____g/cm3 (�г�����ʽ���ɣ���NA ��ʾ����٤��������ֵ)��
���𰸡� 1 ![]() ACDE
ACDE ![]() ��
��![]() �������� sp3 K 4Fe(CN) 6 + 6H 2SO 4 + 6H 2O
�������� sp3 K 4Fe(CN) 6 + 6H 2SO 4 + 6H 2O![]() 2K 2SO 4 + FeSO 4 +3(NH 4) 2SO 4 +6CO��
2K 2SO 4 + FeSO 4 +3(NH 4) 2SO 4 +6CO�� ![]()
��������(1)��̬��ԭ�Ӻ�������Ų�ʽΪ1s22s22p63s23p64s1��������ߵĵ��������ܼ��Ĺ����ĿΪ1����Ϊ26��Ԫ�أ�Fe2+�ĺ�������Ų�ʽΪ1s22s22p63s23p63d6����Χ�����Ų�ͼΪ![]() ���ʴ�Ϊ��1��
���ʴ�Ϊ��1��![]() ��
��
(2)K4[Fe(CN)6]Ϊ���ӻ�����������Ӽ�����[Fe(CN)6]4- �У�һ�� CN-�к���1������2��������C��N�Dz�ͬ��ԭ������Ϊ���Լ�����֮��Ϊÿ��CN-��Fe������λ�����ϣ������Ǽ��Լ�,��ѡ��ACDE��
(3)��CN-��Ϊ�ȵ������������C22-�ȣ�����ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(4)�������PO43-��Pԭ�ӵļ۲���Ӷ���Ŀ=4������sp3�ӻ����ռ乹��Ϊ�������壬�������辧����ÿ����ԭ����Χ��4��Oԭ�ӣ���ԭ�ӵļ۲���Ӷ���Ŀ=4������sp3�ӻ����ʴ�Ϊ���������壻sp3��
(5)��Ѫ����Һ��ϡ�������ʱ������������ԭ��Ӧ��˵��Ԫ�ػ��ϼ۲��䣬���������κ�һ����CN-�ǵȵ��������̬���������Ԫ���غ�֪����̬��������CO����Ԫ�ش��������������У���Ԫ�ش�����������У����Ը÷�Ӧ����ʽΪ��K4Fe(CN)6+6H2SO4+6H2O![]() 2K2SO4+FeSO4+3(NH4)2SO4+6CO�����ʴ�Ϊ��K4Fe(CN)6+6H2SO4+6H2O
2K2SO4+FeSO4+3(NH4)2SO4+6CO�����ʴ�Ϊ��K4Fe(CN)6+6H2SO4+6H2O![]() 2K2SO4+FeSO4+3(NH4)2SO4+6CO����
2K2SO4+FeSO4+3(NH4)2SO4+6CO����
(6)Fe0.9O����ľ����ṹΪNaCl�ͣ�����ÿ�������к���4��Oԭ�ӣ���4����Fe0.9O�����ٸ���m=��V��֪��4��(56��0.9+16)g=��(4.28��10-8 cm)3 NA�������=![]() g/cm3���ʴ�Ϊ��
g/cm3���ʴ�Ϊ�� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������ء�������Ʒ���Ӧ�IJ�����ƥ�����
A. ���ά���������β��� B. ������ƿ�����Ͻ����
C. ����֯����ϳ���ά���� D. ����̥�����л��߷��Ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ձ��ע�����⣬�������ʲ������������ָ����Ҫ��Ⱦ�����
A.��������B.������̼C.PM2.5D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Դ�����ù����У���ֱ�Ӳ���CO2����
A. ʯ�� B. ̫���� C. ���� D. ��Ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ��������ˮϡ��1mol/L�Ĵ�����Һ��0.01mol/L������Һ��ϡ�ͣ����и�����ʼ�ձ����������Ƶ��ǣ�������
A.![]()
B.![]()
C.![]()
D.![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ӡˢ��·�壨���PCB���ǵ��Ӳ�Ʒ����Ҫ��ɲ��֣���PCB�ļӹ������У������ü���ʴ�̷���ʴ�̺�ķ�Һ�д��ڴ�����[Cu(NH3)4]C12�����ֱ���ŷŲ��������Դ�˷ѣ�������Ⱦ��������ͼ�Ǽ���ʴ����PCB��������ʴ�̷�Һ�Ƽ�ʽ̼��ͭ��Cu2(OH)2CO3���Ĺ������̡�

��1������ʴ��ʱ������Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��2����Һa��������Ҫ��__________������ѧʽ��
��3����ͬ�İ�ͭ�Ⱥ�̼ͭ���������ܽ�CuO��A��Һ��ʵ��������ͼ���÷�Ӧ�����ʵ������Ϊ_______________________________������ͭ��ָn(NH3)��n(CuO)��̼ͭ��ָn(NH4HCO3)��n(CuO) ��

��4��A��Һ��Ҫ��[Cu(NH3)n]2+������Һ����������ˮ̼���ν��з������Ԫ����������ΪN��17.5%��Cu��39.7%�������ɫ����Ļ�ѧʽ��____________��
��5��д�����������Ӧ�Ļ�ѧ����ʽ__________________________________________��
��6������ʱ�����ѡ���ڳ�ѹ80�������½��У���ʹ��Ӧ24Сʱ��Ҳ�����������������Ҳ�Cu2(OH)2CO3����������ԭ��Ϊ______________________________________��
��7���������б����ѭ��ʹ�õ������⣬����ѭ��ʹ�õ�������__________��
��8����֪ij��ʵ���0.4L ��CuԪ��140g/L��ʴ�̷�Һ��ü�ʽ̼��ͭ82.5g����CuԪ�ػ�����Ϊ_____________�����������1%����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ��� K+��NH4+��Ca2+��Cl�C��SO42�C��CO32�C�е������֡�Ϊ��ȷ������Һ����ɣ�ȡ100mL������Һ����������ʵ�飺(�����Լ�������������ȫ���ݳ�)����˵������ȷ����
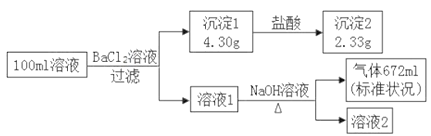
A. ԭ��Һ��һ������SO42�C��CO32�C��NH4+
B. ԭ��Һ��һ��������Ca2+�����ж�Cl�C�Ƿ����
C. Ҫȷ��Cl�C�Ƿ���ڣ���ȡ������Һ2������������ϡ�������
D. ԭ��Һ�� c(K+ )��0.1 mol�� L�� 1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ����H1=��393.5 kJ�� mol-1����H2=��395.4kJ�� mol-1������˵�����ʾʽ��ȷ����

A. C��s��ʯī��== C��s�����ʯ�� ��H= +1.9 kJ�� mol-1
B. ʯī�ͽ��ʯ��ת���������仯
C. ���ʯ���ȶ���ǿ��ʯī
D. ʯī���ܼ��ܱȽ��ʯ���ܼ���С1.9 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���κ�һ����ѧ��Ӧ�ж�����������仯�����ʱ仯��
��1����������ӷ�Ӧ��Fe +Cu2+==Fe2++ Cu�����һ��ԭ��ء��������ҺΪ______��д�������缫��Ӧʽ��______��
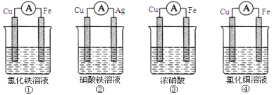
��2��Ϊ����֤ Fe3+�� Cu2+������ǿ��������װ���ܴﵽʵ��Ŀ�ĵ���______��
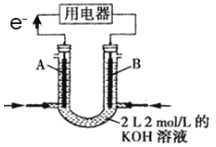
��3���� H2��Ƴ�ȼ�ϵ�أ����������ʱ�ֱ��ȼ�ո��ߣ�װ������ͼ��ʾ��A�� B Ϊ���̼������______���缫���ͨ H2���� A �� B������缫��ӦʽΪ______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com