
【题目】Q、W、X、Y、Z 是位于不同主族的五种短周期元素,其原子序数依次增大。
①W 的氢化物与 W 最高价氧化物对应水化物反应生成化合物甲。
②X、Y、Z 的最高价氧化物对应水化物之间两两反应均可生成盐和水。
③常温下,Q 的最高价气态氧化物与化合物 X2O2 发生反应生成盐乙。
请回答下列各题:
(1)甲的水溶液呈酸性,用离子方程式表示其原因____________________________________________________________________________。
(2)③中反应的化学方程式为________________________________________________________________________________________________。
(3)已知:ZO3n-+M2++H+→Z-+M4+ + H2O(M 为金属元素,方程式未配平)由上述信息可推测 Z 在周期表中位置为________________________________________________________________________________________________。
(4)Y 形成的难溶半导体材料 CuYO2 可溶于稀硝酸,同时生成 NO。写出此反应的离子方秳式_____________________________。
【答案】NH4++H2O![]() NH3·H2O+H+ 2Na2O2+2CO2=2Na2CO3+O2 第三周期第ⅦA 族 16H++3CuAlO2+NO3-=3Cu2++ 3Al3++NO+ 8H2O
NH3·H2O+H+ 2Na2O2+2CO2=2Na2CO3+O2 第三周期第ⅦA 族 16H++3CuAlO2+NO3-=3Cu2++ 3Al3++NO+ 8H2O
【解析】
根据题干可知 Q、W、X、Y、Z 分别为 C、N、O、Na、Cl 五种元素。
(1)甲为硝酸铵,其水溶液呈酸性,主要是铵根水解显酸性,其离子方程式表示其原因NH4++H2O![]() NH3·H2O+H+。
NH3·H2O+H+。
(2)③中反应为二氧化碳和过氧化钠反应生成碳酸钠和氧气,其化学方程式为2Na2O2+2CO2=2Na2CO3+O2。
(3)根据方程式ZO3n- →Z-,由上述信息可推测Z为Cl,在周期表中位置为第三周期第ⅦA 族。
(4)Y形成的难溶半导体材料 CuYO2 可溶于稀硝酸,同时生成NO。此反应的离子方程式为16H++3CuAlO2+NO3-=3Cu2++ 3Al3++NO+ 8H2O。
(1)甲为硝酸铵,其水溶液呈酸性,主要是铵根水解显酸性,其离子方程式表示其原因NH4++H2O![]() NH3·H2O+H+,故答案为:NH4++H2O
NH3·H2O+H+,故答案为:NH4++H2O![]() NH3·H2O+H+。
NH3·H2O+H+。
(2)③中反应为二氧化碳和过氧化钠反应生成碳酸钠和氧气,其化学方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2。
(3)根据方程式ZO3n- →Z-,由上述信息可推测Z为Cl,在周期表中位置为第三周期第ⅦA 族,故答案为:第三周期第ⅦA 族。
(4)Y形成的难溶半导体材料 CuYO2 可溶于稀硝酸,同时生成NO。此反应的离子方程式为16H++3CuAlO2+NO3-=3Cu2++ 3Al3++NO+ 8H2O,故答案为:16H++3CuAlO2+NO3-=3Cu2++ 3Al3++NO+ 8H2O。


科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)
A.  用于检验溴乙烷消去生成的乙烯
用于检验溴乙烷消去生成的乙烯
B.  用于石油的分馏
用于石油的分馏
C.  用于实验室制硝基苯
用于实验室制硝基苯
D. 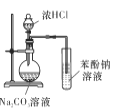 可证明酸性:盐酸>碳酸>苯酚
可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车内燃机燃烧时,在高温引发氮气和氧气反应会产生 NOx 气体,NOx 的消除是科研人员研究的重要课题。
(1)通过资料查得 N2(g)+O2(g)2NO(g)△H反应温度不平衡常数的关系如下表:
反应温度/℃ | 1538 | 2404 |
平衡常数 |
|
|
则△H___________________0(填“<”“>”戒“=”)
(2)在 800℃时,测得 2NO(g)+O2(g) 2NO2(g)的反应速率不反应物浓度的关系如下表所示
初始浓度/ | 初始速率/ | |
C0(NO) | C0(O2) | |
0.01 | 0.01 |
|
0.01 | 0.02 |
|
0.03 | 0.02 |
|
已知反应速率公式为 V 正=K 正×c m(NO)cn(O2),则 m=___________________, K 正=___________________L2mol-2s-1
(3)在某温度下(恒温),向体积可变的容器中充人 NO2 气体,发生反应 2NO

①该反应的压力平衡常数 KP=___________________。
②4s 时压缩活塞(活塞质量忽略不计)使容器体积变为原体积的 1/2,6s 时重新达到平衡,则P(N2O4)=___________________kPa。
(4)某学习小组利用图 2 装置探究向汽车尾气中喷入尿素溶液处理氮的氧化物。则该装置工作时,NO2 在 b 电极上的电极反应式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学元素形成的单质或化合物在工农业生产、军事国防、医疗生活各个领域发挥着重要的作用。
(1)钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82—+8H2O![]() 2MnO4—+10SO42—+16H+
2MnO4—+10SO42—+16H+
①基态S原子核外有____种不同空间运动状态的电子。
②已知H2S2O8的结构如图所示:

H2S2O8中硫原子的轨道杂化方式为________;上述反应每生成1molMnO4—,S2O82—断裂的共价键类型及其数目分别为________、__________(设阿伏伽德罗常数的值为NA)
(2)Fe可以与CN—、H2NCONH2(尿素)等多种配体形成配合物。
①请写出与CN—互为等电子体的一种分子:______、一种离子:_________。
②组成尿素的第二周期元素的第一电离能由大到小的顺序为:________,1molH2NCONH2(尿素)分子中含有σ键的数目为_______。
③FeN的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或b位置Fe,形成Cu替代型产物Fe(x—n)CunNy。

Cu处于周期表中_____区,其最高能层的符号为____,基态铜原子的价电子排布式为________。FexNy转化为两种Cu的替代型产物的能量变化如图2所示,其中相对不稳定的Cu替代型产物的化学式为_________。
(3)铬是银灰色的结晶体,质硬而脆,是制造不锈钢、高速钢的重要原料。
①CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是____(填“极性”或“非极性”)分子
②CrCl3·6H2O实际上是配合物,配位数是6,其固体有三种颜色,其中一种浅绿色固体于足量硝酸银反应时,1mol固体可生成1molAgCl沉淀,则这种浅绿色固体中阳离子的化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 A 含有碳、氢、氧三种元素,其质量比是 3:1:4,B 是最简单的芳香烃,D 是有芳香气味的酯。它们之间的转换关系如下:
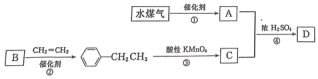
回答下列问题:
(1)A 的结构简式为__________________________________________。
(2)C 中的官能团为__________________________________________。
(3) ![]() 的一氯代物有_________________________________________种。(不考虑立体异构)
的一氯代物有_________________________________________种。(不考虑立体异构)
(4)反应④的化学方程式为______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素X、Y、Z、M、N、O、P,原子序数逐渐增大,其中X、Y、Z、M、N为短周期元素,而X、Y、Z、M处于同周期的P区,且未成对电子数之比为1:2:3:2;N与Z同族。O、P分别位于周期表第2、4列,P的单质被称为“未来金属”,具有质量轻、强度大、耐腐蚀性好的优点。
(1)Y、Z、M三种元素的电负性由大到小的顺序:________(用元素符号表示)。
(2)M的常见氢化物的氢键的键能小于HF的氢键的键能,但Z的常见氢化物常温下为液态而HF常温下为气态的原因是:__________。
(3)XN一种耐磨涂料,可用于金属表面保护层,该化合物可由X的三溴化物和N的三溴化物于高温下在氢气的氛围中合成。
①写出合成XN的化学方程式:_________。(各物质用化学式表示)
②XN的晶体的晶胞如图所示:
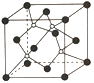
其中实心球为N,在一个晶胞中N原子空间堆积方式为______,N原子的配位数为______;该结构中有一个配位键,提供空轨道的原子是________(写元素符号)。
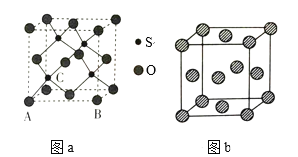
(4)O和硫形成的某种晶体的晶胞如图a所示:该晶胞原子的坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为_______。
(5)图b为P的一种面心立方晶胞结构,若晶胞的边长为anm,则P的密度为_____g·cm-3(用含a和NA的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型冠状病毒对紫外线和热敏感,有些方法还是可以有效灭活病毒的,下列说法错误的是
A.疫苗一般应冷藏存放
B.75%的酒精杀菌消毒的原理是使蛋白质变性
C.含氯消毒剂(如84消毒液)使用过程中有化学反应发生
D.过氧乙酸(CH3COOOH)中氧原子的杂化方式为sp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
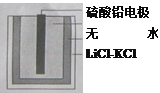
A.正极反应式:Ca+2Cl- - 2e-= CaCl2
B.常温时,在正负极间接上电流表或检流计,指针不偏转
C.放电过程中,Li+向负极移动
D.每转移0.1mol电子,理论上生成20.7g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是
A.等体积、等物质的量浓度的NaCl(aq) 离子总数大于NaClO(aq)中离子总数
B.pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度
C.0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
D.向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com