
| A.①④⑥ | B.①②③④⑤ | C.①④ | D.①②③ |


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.③④⑤⑥ | C.①③⑥ | D.③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子键就是使阴、阳离子结合成化合物的静电引力 |
| B.所有金属与所有非金属之间都能形成离子键 |
| C.在化合物CaCl2中,两个氯离子之间也存在离子键 |
| D.含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. Na2O 和 SiO2 | B.冰和金刚石熔化 |
| C.氯化钠和蔗糖熔化 | D.碘和干冰升华 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中只能含有离子键 |
| B.共价化合物中只能含有共价键 |
| C.活泼金属元素和非金属元素之间一定以离子键结合 |
| D.化学键不仅存在于原子之间,也存在于分子之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
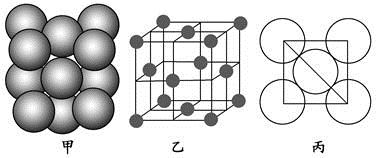
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只含有共价键的物质不一定是共价化合物 |
| B.由电子定向移动而导电的物质一定是金属晶体 |
| C.有键能很大的共价键存在的物质熔沸点一定很高 |
| D.原子晶体中只存在非极性共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中一定含有离子键 |
| B.单质分子中均不存在化学键 |
| C.非极性共价键不可能存在于离子化合物中 |
| D.含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强 |
| B.在氯化钠中,氯离子和钠离子靠静电作用结合 |
| C.任何离子键在形成的过程中必定有电子的得与失 |
| D.金属钠与氯气反应生成氯化钠后,体系能量降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com