
A.2 mol B.3 mol C.4 mol D.5 mol
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源:2013-2014学年高考化学二轮专题冲刺第8讲 电化学基础练习卷(解析版) 题型:填空题
(1)如图1是一种新型燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验。
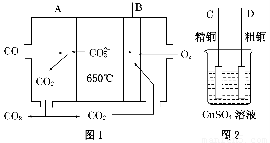
回答下列问题:
①写出A极发生的电极反应式______________________________________。
②要用燃料电池为电源进行粗铜的精炼实验,则B极应与________极相连(填“C”或“D”)。
③当消耗标准状况下2.24 L CO时,C电极的质量变化为________。
(2)工业上,可用铁作阳极,电解KOH溶液制备K2FeO4。
①电解过程中,OH-向________(填“阴”或“阳”)极移动,阳极的电极反应式为____________________________。
②若阳极有28 g Fe溶解,则阴极析出的气体在标准状况下的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com