
【题目】废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH4+完全转化为N2,该反应可表示为2NH![]() +3ClO-===N2↑+3Cl-+2H++3H2O。下列说法中不正确
+3ClO-===N2↑+3Cl-+2H++3H2O。下列说法中不正确
A. 反应中氮元素被氧化,氯元素被还原
B. 还原性:NH4+>Cl-
C. 反应中每生成1 mol N2,转移6 mol电子
D. 经此法处理过的废水可以直接排放
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
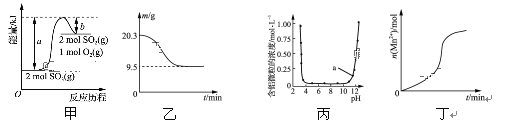
A. 由图甲可知,2SO3(g)![]() 2SO2(g)+O2(g) ΔH=(b-a)kJ·mol-1
2SO2(g)+O2(g) ΔH=(b-a)kJ·mol-1
B. 图乙表示0.1 mol MgCl2·6H2O在空气中充分加热时残留固体质量随时间的变化
C. 图丙表示Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中存在大量Al3+
D. 图丁表示10 mL 0.01 mol·L-1酸性KMnO4溶液与过量的0.1 mol·L-1的H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对反应有催化作用)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近发现两种粒子:第一种是由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子。下列有关这两种粒子的说法正确的是
A. “四中子”的粒子不显电性 B. “四中子”的电子数为4
C. 第二种粒子是氧元素的另一种同位素 D. 第二种粒子是一种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬(Cr2O3)主要用于冶炼金属铬、有机化学合成的催化剂等。工业上是以铬铁矿[主要成份为Fe(CrO2)2,还含有Al2O3、SiO2等杂质]为主要原料进行生产,其主要工艺流程如下:
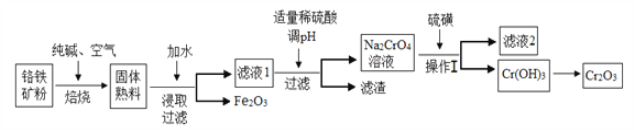
(1)亚铬酸亚铁[Fe(CrO2)2]中Cr的化合价是___________。
(2)焙烧时的主要反应为:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2,该步骤不能使用陶瓷容器,原因是____________________________________。
8Na2CrO4+2Fe2O3+8CO2,该步骤不能使用陶瓷容器,原因是____________________________________。
(3)操作I包括过滤与洗涤,简述实验室中洗涤沉淀的操作:___________________________。
(4)硫磺在与铬酸钠的反应中转化为硫代硫酸钠,反应的离子方程式为________________________。滤渣中除Al(OH)3外还有__________(填化学式)。
(5)某工厂用448 kg铬铁矿粉[含Fe(CrO2)280%]制备Cr2O3,最终得到产品182.4 kg,产率为______%。
(6)Cr3+也有一定毒性,会污染水体,常温下要除去废液中多余的Cr3+,调节pH至少为_______,才能使铬离子沉淀完全。(已知溶液中离子浓度小于1×10-5 mol·L-1,则认为离子完全沉淀;Cr(OH)3的溶度积常数为1.0×10-32。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(CN)2、(OCN)2、(SCN)2等通称为拟卤素,它们的性质与卤素相似,氧化性强弱顺序是:F2>(OCN)2>Cl2>(CN)2>(SCN)2>I2下列方程式中错误的是( )
A.2NaSCN+MnO2+2H2SO4=Na2SO4+(SCN)2↑+MnSO4+2H2O
B.(CN)2+2KI=2KCN+I2
C.Cl2+2NaOCN=(OCN)2+2NaCl
D.2AgCN=2Ag+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氯气与碱的反应中,氯气表现酸性
B.工业上制取漂白粉时使用石灰水可以使反应更充分
C.洁厕灵和漂白液混合使用即可起到清污作用又可起到杀菌作用
D.实验室对含有氯气的尾气可用氢氧化钠溶液吸收处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
①CH3Cl ② ![]() ③
③ ![]() ④
④![]()
A. ①② B. ②③④ C. ② D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在学习了元素周期律之后,某化学实验小组设计了如下实验,验证碳元素的非金属性比硅元素的非金属性强,请回答下列问题:
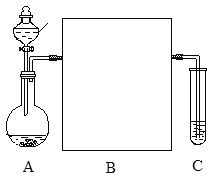
(1)装置A的分液漏斗中盛装的试剂是_____,烧瓶中加入块状固体是_____。
(2)装置C中盛放的试剂是_____(选填字母)
A.Na2CO3溶液 B.Na2SiO3溶液 C.NaOH溶液
(3)画出实线框内的实验装置图,并注明所加试剂,该装置的作用是_____,
(4)C中实验现象为_____,化学反应方程式是_____。若没有B装置,虽然C中出现的现象相同,但也不能得出正确结论,原因是_____。
(5)从碳、硅在周期表中的位置角度,简要分析碳元素的非金属性比硅元素的非金属性强的原因是_____。
(6)还有哪些事实能够说明碳元素的非金属性比硅元素的非金属性强(试举一例)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com