
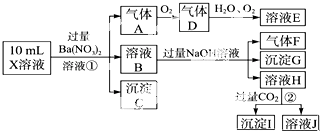
分析 在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,不能确定是否含有的离子Fe3+和Cl-,以此解答.
解答 解:在强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,不能确定是否含有的离子Fe3+和Cl-,
(1)由以上分析可知一定不存在CO32-、SO32-、NO3-,故答案为:CO32-、SO32-、NO3-;
(2)①Fe2+离子被氧化为Fe3+离子,反应的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)A、F、I均为0.01mol,10mL X溶液中n(H+)=0.04mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知Fe2+物质的量为0.03mol; 溶液中正电荷为:2n(Fe2+)+3n(Al3+)+n(NH4+)+n(H+)=2×0.03mol+3×0.01mol+0.01mol+0.04mol=0.14mol;沉淀C为硫酸钡,其物质的量0.07mol,n(SO42-)=0.07mol,硫酸根离子所带的负电荷为:0.07mol×2=0.14mol,说明溶液中正负电荷相等,所以若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等,
故答案为:若检验Fe3+肯定存在时,就有Cl-存在,因肯定存在的离子电荷总数已相等.
点评 本题考查无机物的推断,根据物质间发生反应的特殊现象结合离子共存来分析解答,熟悉物质的性质是解本题关键,根据溶液和硝酸钡反应生成气体确定溶液中存在亚铁离子,为解答本题的易错点,熟练掌握离子共存的条件,灵活运用知识解答,题目难度中等.


科目:高中化学 来源: 题型:解答题
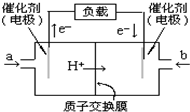 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.反应时释放大量热并快速产生大量气体.已知在101kPa,298K时,1mol液态N2H4在氧气中完全燃烧生成N2和水蒸气,放出热量624kJ,该反应的热化学方程式是N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=-624KJ/mol.又知:H2O(g )=H2O (l)△H=-44kJ•mol-1,若1mol液态N2H4在氧气中完全燃烧生成N2和液态水,则放出热量为712kJ.
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.反应时释放大量热并快速产生大量气体.已知在101kPa,298K时,1mol液态N2H4在氧气中完全燃烧生成N2和水蒸气,放出热量624kJ,该反应的热化学方程式是N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=-624KJ/mol.又知:H2O(g )=H2O (l)△H=-44kJ•mol-1,若1mol液态N2H4在氧气中完全燃烧生成N2和液态水,则放出热量为712kJ.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3的熔点高,可用作耐火材料 | |
| B. | NaHCO3与盐酸反应,可用于治疗胃酸过多 | |
| C. | SO2可污染环境,不可用于杀菌、消毒 | |
| D. | 二氧化氮、氨气、氯气和二氧化硫都是易液化的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把30℃的硝酸钾饱和溶液加热到60℃,溶液的质量分数和物质的量浓度均增大 | |
| B. | 把60℃的硝酸钾饱和溶液降温到30℃,溶液仍饱和,溶液的质量分数和物质的量浓度均不变 | |
| C. | 60℃硝酸钾饱和溶液中含有的溶质的质量比30℃的硝酸钾饱和溶液中多 | |
| D. | 把30℃的硝酸钾饱和溶液加热到60℃,溶液的质量分数和物质的量浓度均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③④ | B. | 只有①②③④⑤ | C. | 只有②③④ | D. | 只有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医用酒精的浓度通常是95% | |
| B. | 淀粉、纤维素、蛋白质和油脂都属于天然高分子化合物 | |
| C. | 用食醋可除去热水壶内壁的水垢 | |
| D. | 生活中常用明矶对水进行处理,起净化、杀菌、消毒作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  是向容量瓶转移溶液 | |
| B. | 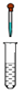 制取氢氧化亚铁 | |
| C. | 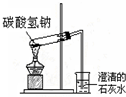 是碳酸氢钠受热分解 | |
| D. | 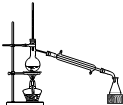 分离四氯化碳(沸点76.75℃)和甲苯(沸点为110.6℃)的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②③ | C. | 只有①③ | D. | 都正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com