
为了除去铁粉中的少量铝粉,可以选取下列哪种溶液( )
|
| A. | 浓盐酸 | B. | 浓硝酸 |
|
| C. | 浓硫酸 | D. | 浓氢氧化钠溶液 |
考点:
铝的化学性质.
专题:
几种重要的金属及其化合物.
分析:
根据铝能与碱反应,而铁不反应,则向粉末中足量加入浓氢氧化钠溶液,反应后过滤即可得到纯净的铁粉.
解答:
解:A、因Fe、Al都与浓盐酸反应,则不能用来除杂,故A错误;
B、因Fe、Al都与浓硝酸反应,且常温下都发生钝化,则不能用来除杂,故B错误;
C、因Fe、Al都与浓硫酸反应,且常温下都发生钝化,则不能用来除杂,故C错误;
D、因Fe不与氢氧化钠溶液反应,但Al能与氢氧化钠溶液反应,则可以利用浓氢氧化钠溶液除去铁粉中的少量铝粉,故D正确;
故选D.
点评:
本题考查除杂,明确Al的化学性质是解答本题的关键,学会利用Fe、Al性质的差异来选择合适的除杂试剂即可解答,难度不大.


科目:高中化学 来源: 题型:
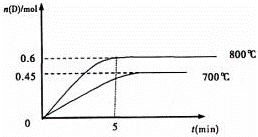
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)⇌C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题:
(1)800℃时.0﹣5min内,以B表示的平均反应速率为 .
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3 )若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= 反应为 填吸热或放热)
)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= 反应为 填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,
n(D)=0.9mol,则此时该反应向 填“向正反应方向”“向逆反应方向”或“处于平衡状态”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
|
| A. | 从1L 1mol•L﹣1的NaCl溶液中取出10mL,其浓度仍是1mol•L﹣1 |
|
| B. | 制成0.5L 10mol•L﹣1的盐酸,需标准状况下氯化氢气体112L |
|
| C. | 0.5L 2mol•L﹣1 BaCl2溶液中,Ba2+和Cl﹣总数为3×6.02×1023 |
|
| D. | 10g 98%硫酸(密度为1.84g•cm﹣3)与10mL 18.4 mol•L﹣1硫酸的浓度是不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
取一定量的Na2CO3、NaHCO3和Na2SO4的混合物与250mL 1.00mol•L﹣1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100mol•L﹣1 Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL,1.00mol•L﹣1盐酸恰好完全中和.
求:
(1)n(CO2)= mol;
(2)m(Na2SO4)= g;
(3)m(NaHCO3)= g.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是( )
①Na2CO3 ②Al2O3 ③Al(OH)3 ④Al.
|
| A. | ③④ | B. | ②③④ | C. | ①③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将Fe,Cu,Fe2+,Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有( )
|
| A. | Cu,Fe3+ | B. | Fe2+,Fe3+ | C. | Cu,Cu2+,Fe | D. | Cu,Fe2+,Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 2A=B+3C,在20℃时进行,v(A)=5mol/(L•s),已知每升温10℃,该反应速率增大到原来的2倍,则当其它条件不变而温度升到50℃时,反应速率v(B)是()
A. 20 mol/(L•s) B. 40 mol/(L•s) C. 60 mol/(L•s) D. 15 mol/(L•s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com