
| A、25°C时,pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA | ||
| B、室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2.0NA | ||
C、1L 0.5mol?L-1 的(NH4)2SO4溶液中含有的N
| ||
| D、标准状况下,22.4LCCl4中含有的共用电子对数目为4.0NA |
| 14g |
| 14g/mol |


科目:高中化学 来源: 题型:
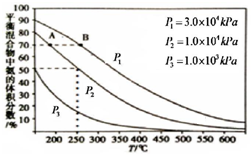 目前工业合成氨的原理是:
目前工业合成氨的原理是:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是国际单位制的一种基本单位 | B、摩尔是表示物质的量的单位 | C、摩尔是以阿伏加德罗常数为衡量标准的物质的量的单位 | D、摩尔是表示物质粒子数量的单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA | B、常温常压下,17g甲基(-14CH3)所含的电子数为9NA | C、同温同压下,1L NO和1L O2充分混合体积小于1.5L | D、pH=l的醋酸溶液100mL中氢离子数为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 1mol?L-1的NH4Cl溶液中一定含有NA个NH4+ | B、常温常压下,22.4L乙烯中含极性共价键数为5NA | C、6.8g熔融的KHSO4中含有0.05NA个阳离子 | D、1mol冰醋酸和1mol乙醇在浓硫酸加热下反应可生成NA个H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,32g甲醇中含有的C-H键的数目为4NA | B、标准状况下,11.2L甲醛中含有的电子数目为8NA | C、0.1mol N2与0.3mol H2在一定条件下充分反应,生成的氨分子数目为0.2NA | D、1L 0.01mol?L-1 KAl(SO4)2溶液中,含有的阳离子数目为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下1.0L 0.1mol?L-1NH4Cl溶液中,NH4+和H+总数大于0.1NA | B、常温下,11.2L乙烯在氧气中完全燃烧转移的电子数为6.0NA | C、88.0g干冰中含有的电子对数为8.0NA | D、1.2g金刚石中含有的碳碳键数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12g NaHSO4固体中含有的离子数为0.3NA | B、足量Cl2与5.6g Fe完全反应时,转移的电子数为0.2NA | C、标准状况下,0.56L丙烷中含有的共价键数为0.25NA | D、电解精炼铜时每转移NA个电子,阳极溶解32g铜 |
查看答案和解析>>
科目:高中化学 来源:2014~2015学年重庆市9月月考高一化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L- 1 KNO3溶液:H+、Fe 2+、SCN -、SO42-
B.pH=0的溶液:Al3+、Cu(NH3)42+、F -、SO42 -
C.c(ClO- )=1.0mol·L- 1的溶液:Na+、SO32 -、S2 -、SO42 -
D.c(H+ )/c(OH - )=10 -10 的溶液:K+、Ba2+、NO3-、Cl -
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com