
| 1.8g |
| 40g/mol |
| 1 |
| 3 |
| 1 |
| 3 |
| 10g |
| 0.015mol |
| 6g |
| 2g/mol |
| 1000g | ||
|
| 1.8g |
| 40g/mol |
| 1 |
| 3 |
| 1 |
| 3 |
| 10g |
| 0.015mol |
| 6g |
| 2g/mol |
| 1000g | ||
|


科目:高中化学 来源: 题型:
 常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是( )
常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是( )| A、曲线I为醋酸稀释时pH值变化曲线 |
| B、a点时,若都加入相同大小的锌粒,此时盐酸反应的速率大 |
| C、a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多 |
| D、b点溶液中水的电离程度比c点溶液中水的电离程度小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中C、H、O原子个数比为14:12:3 |
| B、它由碳、氢、氧三种元素组成 |
| C、该物质中,碳、氢、氧三种元素的质量比为14:12:3 |
| D、它的摩尔质量为228g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(B) |
| c(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |

| 实验编号 | 窗口体积/L | 温度/℃ |
| ① | 1.0 | 1200 |
| ② | 2.0 | 1200 |
| ③ | 2.0 | 1300 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Cu2O/ZnO |
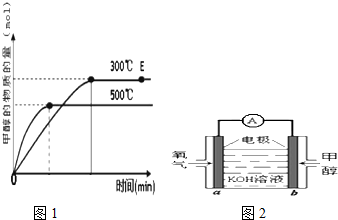
| 1 |
| 2 |
| c(CH3OH) |
| c(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
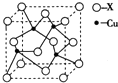 (1)HCNO是一种弱酸,它的酸性类似于醋酸,在水中微弱地电离出H+和CNO-.
(1)HCNO是一种弱酸,它的酸性类似于醋酸,在水中微弱地电离出H+和CNO-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com