
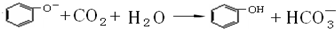 ,该反应说明苯酚具有的性质是弱酸性.
,该反应说明苯酚具有的性质是弱酸性. 分析 (1)C6H5OH与NaOH反应生成易溶于水的C6H5ONa,为中和反应;
(2)C6H5ONa溶液中通入CO2,生成苯酚沉淀.
解答 解:(1)苯酚与水混合,溶液变浑浊,向该浊液中滴加NaOH溶液,可观察到的现象是溶液变澄清,反应的化学方程式为C6H5OH+NaOH→C6H5ONa+H2O,该反应说明苯酚具有酸性,
故答案为:溶液变澄清;C6H5OH+NaOH→C6H5ONa+H2O;酸;
(2)向上述溶液中通入CO2,发生的离子反应为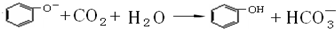 ,可观察到的现象是溶液变浑浊,该反应为强酸制取弱酸的反应,说明苯酚具有的性质是具有弱酸性,
,可观察到的现象是溶液变浑浊,该反应为强酸制取弱酸的反应,说明苯酚具有的性质是具有弱酸性,
故答案为:溶液变浑浊;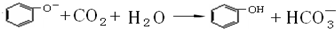 ;弱酸性.
;弱酸性.
点评 本题考查有机物的结构与性质,为高频考点,把握苯酚的酸性、强酸制取弱酸的原理等为解答的关键,侧重分析与应用能力的考查,注意酚的性质及应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
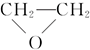 ③CH3CHO;④
③CH3CHO;④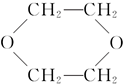 ⑤HO-CH2CH2OCH2CH2-OH.
⑤HO-CH2CH2OCH2CH2-OH.| A. | 只有① | B. | 只有①④ | C. | 只有①⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{b-a}{V}$ mol•L-1 | B. | $\frac{2b-a}{V}$mol•L-1 | C. | $\frac{b-a}{V}$mol•L-1 | D. | $\frac{2(2b-a)}{V}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:H2S>HF | B. | HCl的电子式为H+Cl- | ||
| C. | 一个D2O分子所含的中子数为8 | D. | 酸性强弱:HClO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
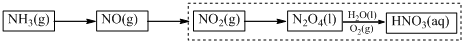
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 1 mol Zn与足量的该硫酸反应产生2 g氢气 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50.0 mL | |
| D. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AsH3的热稳定性大于H2S | B. | 砷的原子半径小于磷的原子半径 | ||
| C. | 砷的电负性大于溴 | D. | 基态砷原子有3个未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com