
【题目】下列各组离子在溶液中能大量共存的是( )
A.Na+、Al3+、Cl﹣、SO42﹣
B.Cu2+、Cl﹣、NO3﹣、OH﹣
C.Ca2+、Na+、CO32﹣、NO3﹣
D.H+、SO42﹣、NO3﹣、OH﹣
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 硅晶体中,有NA个Si就有2 NA个Si—Si键
B. 常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中Na+数目相等
C. 惰性电极电解食盐水,若线路中通过2 NA个电子的电量时,则阳极产生气体22.4 L
D. 标准状况下,2 mol Na2O2与44.8 L SO2完全反应,转移的电子数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na2O和Na2O2的叙述正确的是( )
A.Na2O与Na2O2均可与水反应生成氢氧化钠,所以都是碱性氧化物
B.Na2O与Na2O2分别与CO2反应的产物完全相同
C.常温下,钠在空气中反应生成过氧化钠
D.在呼吸面具中,Na2O2常作供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,对于该溶液,下列叙述中正确的是
A. 水电离出来的c(H+)=1×10-10mo1·L-1
B. 此时水的离子积KW=1×10-4
C. c(H+)=2[c(OH-)+c(SO42-)]
D. 该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂。

下列关于实验现象的解释或结论正确的是
选项 | 实验现象 | 解释或结论 |
A | a中无明显现象 | Na2SO3和H2O2一定不发生反应 |
B | b中加稀H2SO4后才产生淡黄色沉淀 | SO32和S2两种离子一定不能大量共存 |
C | c中加BaCl2溶液后产生白色沉淀且红色褪去 | Ba2++ SO32 == BaSO3↓,使SO32水解平衡逆向移动,红色褪去 |
D | d中产生白色沉淀 | 原Na2SO3溶液中含有SO42 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列古诗词的描述中发生的是化学变化的是( )
A.千淘万漉虽辛苦,吹尽狂沙始到金
B.忽如一夜春风来,千树万树梨花开
C.春蚕到死丝方尽,蜡炬成灰泪始干
D.日照香炉生紫烟,遥看瀑布挂前川
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 往氢氟酸溶液中加水稀释时,c(F-)/c(H+) 增大
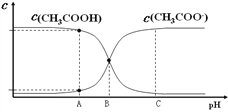
B. 25℃时,0.010 0 mol·L-1 CH3COOH 溶液中,调节溶液pH(忽略体积变化),得到c(CH3COOH) 和 c(CH3COO-)与溶液pH的变化关系如右图所示,A、B、C三点中B对应的溶液抗外界酸、碱的能力最强
C. 将同浓度的Na2CO3、NaHCO3溶液混合后其溶液一定存在2c(H+)+3c(H2CO3)+c(HCO3-)=c(CO32-)+2c(OH-)
D. 已知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为 5.6×10-5 mol·L-1,则生成沉淀所需Na2CO3溶液的最小浓度为 5×10-5 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com