
分析 (1)10s内△c(B2)=0.1mol•L-1,带入v(B2)=$\frac{△c({B}_{2})}{△t}$计算,然后根据化学反应速率之比等于化学计量数之比计算v(C);
(2)根据参加反应的A2和B2的浓度相同,故二者平衡浓度之差应等于起始浓度之差,依此进行计算;平衡从正向和逆向分别建立,依此利用三段式进行计算.
解答 解:(1)10s内△c(B2)=0.1mol•L-1,v(B2)=$\frac{0.1mol•L{\;}^{-1}}{10s}$=0.01mol•L-1•s-1,v(C)=2v(B2)=2×0.01mol•L-1•s-1=0.02 mol•L-1•s-1,
故答案为:0.02 mol•L-1•s-1;
(2)A2(g)+B2(g)?2C(g),参加反应的A2和B2的浓度相同,故二者平衡浓度之差应等于起始浓度之差,即a-b=0.4-0.1=0.3,
若平衡从正向建立,则
A2(g)+B2(g)?2C(g)
起始:a b 0
转化:a-0.4 b-0.1 1.6
平衡:0.4 0.1 1.6
$\frac{a-0.4}{1.6}$=$\frac{1}{2}$,a=1.2mol/L,
若平衡从逆向建立,则
A2(g)+B2(g)?2C(g)
起始:a 0 c
转化:0.1 0.1 0.2
平衡:0.4 0.1 1.6
a+0.1=0.4,a=0.3mol/L,
故a的取值范围为:0.3≤a≤1.2
故答案为:a-b=0.3;0.3≤a≤1.2.
点评 本题考查化学反应速率、化学平衡的相关计算,题目难度中等,要注意运用三段式进行计算.


科目:高中化学 来源: 题型:选择题
| A. | △H1,△H2都不变 | B. | △H1,△H2都增大 | C. | △H1,△H2都减小 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 禁止用工业酒精配制饮用酒和调味用的料酒 | |
| D. | 溴乙烷、TNT、丙三醇都是无色溶于水的有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA | |
| B. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| C. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| D. | 常温下,4gCH4含有NA 个C-H共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn是正极,Ag2O是负极 | |
| B. | 工作时电子由Zn极经溶液移向Ag2O极 | |
| C. | 该电池可将化学能100%转化为电能 | |
| D. | Zn是负极,反应为Zn-2 e-+2OH-=Zn(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
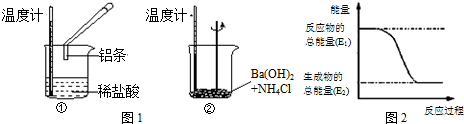
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 是原子半径最小的元素 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 是短周期元素中原子半径最大的主族元素. |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
| F | 原子有三个电子层,且最外层电子数是最内层电子数的3倍, |
 ;
;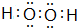 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管在装酸液前用标准盐酸溶液润洗2~3次 | |
| B. | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | |
| C. | 酸式滴定管读数时,滴定前正确读数,滴定后俯视读数 | |
| D. | 盛NaOH溶液的锥形瓶滴定前未干燥,带有水珠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com