
【题目】(Ⅰ)下图中,P为一可自由滑动的活塞,关闭K,分别向容器A、B中各充入1 mol X、1 mol Y,起始时,VA=a L,VB=0.8a L(连通管的体积忽略不计),在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:3X(g)+3Y(g)![]() 2Z(g)+2W(g),达平衡时,VB=0.6a L。回答下列问题:
2Z(g)+2W(g),达平衡时,VB=0.6a L。回答下列问题:
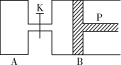
(1)达到平衡时B中X的转化率为________________。
(2)平衡时A、B中混合气体的平均相对分子质量的关系是:MA____________MB(填“>”、“=”或“<”)。
(3)打开K,一段时间后反应再次达到平衡,则B的体积为____________L。
(Ⅱ)工业中采用适当的催化剂利用反应CO(g)+2H2(g)![]() CH3OH(g)来制取甲醇。
CH3OH(g)来制取甲醇。
(4)维持体系的压强一定,温度为T时,在体积为2.0 L的封闭容器内充入0.6 mol CO和0.4 mol H2,达到平衡时含有0.15 mol CH3OH(g),则该反应平衡常数K=________(保留两位小数),此时向容器中再通入0.7 mol CO气体,则此平衡将____________(填“正向”、“不”或“逆向”)移动。
【答案】(Ⅰ)(1)75% (2)< (3)0.2a (Ⅱ)(4)65.33 逆向
【解析】
试题分析::(1)B为恒温恒压,反应前后体积之比等于物质的量之比,令平衡后B中混合气体的物质的量为n,则:0.8aL:0.6aL=2mol:n,解得n=1.5mol。
3X(g)+3Y(g)![]() 2Z(g)+2W(g),
2Z(g)+2W(g),
起始量(mol)1 1 0 0
转化量(mol)x x x/3 x/3
平衡:(1-x)+(1-x)+2x/3+2x/3=1.5
解得x=0.75
所以达到平衡时B中X的转化率为75%;
(2)A为恒温恒容条件,B为恒温恒压条件,B容器体积减小,压强增大,平衡正向进行,气体物质的量减小,混合气体质量不变,根据M=m/n可判断得MA<MB;
(3)打开K达到平衡时,混合气体压强应该与第一次平衡时B的压强相同,该反应是在等温等压条件下进行的反应,AB中反应开始物质的量是4mol,等温等压下,气体的物质的量之比等于体积之比,则打开K时达到平衡状态容器体积应该是原来B容器体积的2倍,为1.2aL,因为VA=a L,则B的体积=1.2aL-aL;
(4) CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始量(mol) 0.6 0.4 0
转化量(mol) 0.15 0.3 0.15
平衡量(mol) 0.45 0.1 0.15
则![]()
解得V=1.4L
所以该反应平衡常数K=
此时向容器中再通入0.7 mol CO气体,则![]() ,解得V1=2.8L
,解得V1=2.8L
此浓度熵Q=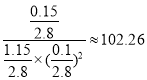 >65.33,所以平衡将逆向移动。
>65.33,所以平衡将逆向移动。


科目:高中化学 来源: 题型:
【题目】利用二氧化碳废气生产化工产品是解决室温效应的有效途径之一,对用二氧化碳为主要原料生产的四种产品(如下图所示)的相关说法不正确的是
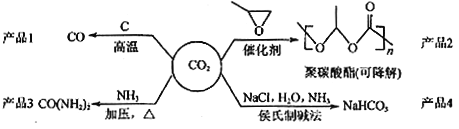
A.反应CO2(g)+C(s)=2CO(g)的△H>0,△S>0
B.用聚碳酸酯代替聚乙烯等传统塑料,可消除白色污染
C.CO(NH2)2与NH4CNO互为同分异构体,两者化学性质相同
D.侯氏制碱法的工艺过程中应用了物质溶解度的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL BaCl2、AlCl3、FeCl3的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如下图所示:
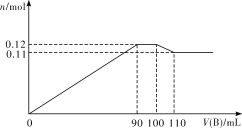
(1)当加入110 mL B溶液时,溶液中的沉淀是___________(填化学式)。
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是___________。当B溶液加到90 mL~100 mL这一段时间中,所发生的离子反应方程式是____________________。
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中。
溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
c/mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O)
C. 3v(NH3)=2v(H2O) D. 5v(O2)=4v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于催化剂的说法,正确的是
A. 催化剂能使不起反应的物质发生反应
B. 催化剂在化学反应前后,化学性质和质量都不变
C. 催化剂不能改变化学反应速率
D. 任何化学反应都需要催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
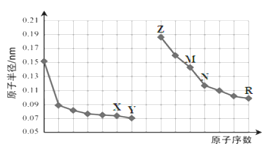
A. X与M形成的一个阴离子中含有29个电子
B. 气态氢化物沸点Y>R
C. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z单质能从M与R元素构成的盐溶液中置换出单质M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A. 利用电池外壳的金属材料
B. 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C. 不使电池中渗泄的电解液腐蚀其他物品
D. 回收其中石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期元素,其中B,C、D、E四种元素在化学反应中均能形成简单的阴、阳离子,且B、C、D离子具有相同的电子层结构。已知:
①A是形成物质种类最多的元素,F和A同主族;
②C的氢化物分子G是具有10电子的微粒,且可以发生下图转化:
![]()
③E和D是同主族元素;
④B和D可形成个数比为1:1和2:1的离子化合物X和Y。
请回答下列问题:
(1)B与D形成离子化合物Y具有漂白性,写出Y的电子式______,该化合物和元素A的最高价氧化物O反应的化学方程式为:__________;一定量的Y与O反应后得到的固体物质,能恰好与含400 mL 2 mol/L的稀盐酸反应,并收集到0.25 mol气体,则该固体物质的组成为________(用物质的量表示)。
(2)G气体的检验方法为_________;13.44 L气体G(标准状况下测定)按照上图转化方式可以获得M物质的量分别为__________mol。
(3)某化学兴趣小组欲采用右图装置证明A、C、F三种元素性质的递变性,其中甲装置中锥形瓶内所加试剂为石灰石:
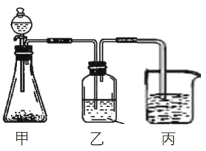
①甲装置中发生反应的离子方程式为________________;
②乙装置中应添加的试剂为______________;
③丙装置中可能发生的实验现象为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,德国科学家利用数亿个镍原子(28Ni)对数亿个铅原子(82Pb)连续轰击数天后,制得一种新原子![]() (暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
(暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
A. 这种原子(![]() )的中子数为169
)的中子数为169
B. 这种元素肯定是金属元素
C. 这种元素属于第6周期元素
D. 这种元素与铅(82Pb)同族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com