
| A、原子半径:O>N>C |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、稳定性:HCl>HI>HBr |
| D、金属性:Al>Mg>Na |


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:
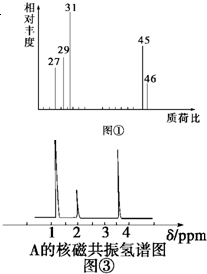 为测定某有机化合物A的结构,进行如下实验:
为测定某有机化合物A的结构,进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:
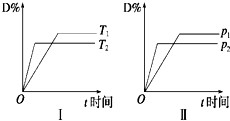 对于可逆反应mA(g)+nB(s)?pC(g)+qD(g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是( )
对于可逆反应mA(g)+nB(s)?pC(g)+qD(g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是( )| A、化学方程式中化学计量数:m>p+q |
| B、降温可使化学平衡向正反应方向移动 |
| C、使用合适的催化剂可使D%有所增加 |
| D、B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
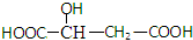 ,下列说法正确的是( )
,下列说法正确的是( )| A、苹果酸中能发生酯化反应的官能团有2种 |
| B、1mol苹果酸可与3mol NaOH发生中和反应 |
| C、1mol苹果酸与足量金属Na反应生成1mol H2 |
D、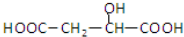 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
| B | CO2(CO) | O2 | 点燃 |
| C | Zn (Cu) | 稀硫酸 | 过滤 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2L 0.5mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
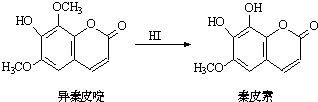 异秦皮啶具有镇静安神抗肿瘤功效,秦皮素具有抗痢疾杆菌功效.它们在一定条件下可发生转化,如图所示.有关说法正确的是( )
异秦皮啶具有镇静安神抗肿瘤功效,秦皮素具有抗痢疾杆菌功效.它们在一定条件下可发生转化,如图所示.有关说法正确的是( )| A、异秦皮啶与秦皮素互为同系物 |
| B、异秦皮啶转化为秦皮素的反应类型为取代反应 |
| C、秦皮素一定条件下能发生加成反应、消去反应和取代反应 |
| D、1mol秦皮素最多可与5molBr2、4molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金(沙子)--过滤 |
| B、NaCl(泥沙)--溶解、过滤、蒸发 |
| C、碘(水)--用酒精萃取 |
| D、NaCl(MgCl2)--加硫酸钠、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
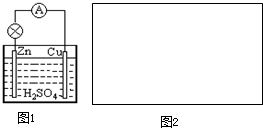 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com