
| A.研制乙醇汽油(汽油中添加一定比例乙醇)技术,不能降低机动车尾气中有害气体排放 |
| B.工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 |
C.为了有效的发展清洁能源,采用电解水的方法大 量制备H2 量制备H2 |
| D.世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体 |

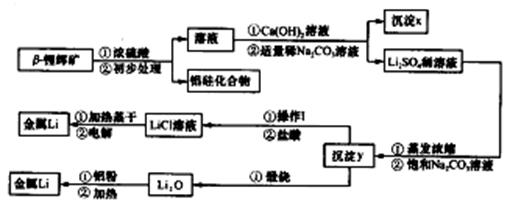
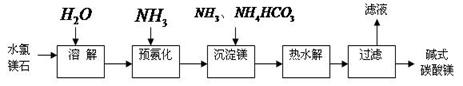
 的流程图。写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 。
的流程图。写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 。
 4 SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于氯碱工业,理论上需消耗纯NaCl的
4 SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于氯碱工业,理论上需消耗纯NaCl的 质量为 kg。
质量为 kg。 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.联合制碱法是将二氧化碳和氨气通入饱和氯化钠溶液中,制得碳酸氢钠,再在高温下灼烧,转化为碳酸钠。 |
| C.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.现代石油化工以乙烯为原料生产环氧化烷的反应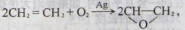 原子利用率为100% 原子利用率为100% |
| B.寻找合适的催化剂可以提高化工生产中反应的原子利用率 |
| C.从根本上解决环境和生态问题,需要依靠“绿色化学”的发展 |
D.CO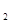 与H 与H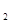 转化为乙烯:2 CO 转化为乙烯:2 CO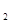 +6 H +6 H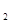  C H C H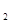 =" C" H =" C" H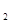 +4 H +4 H O,反应的原子利用率为28% O,反应的原子利用率为28% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“接触法”制H2SO4过程中,选择98%的浓硫酸作为SO3的吸收剂 |
B.海水提镁的主要步骤为: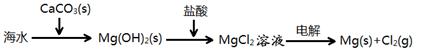 |
| C.侯德榜制碱法最终制得的是纯碱 |
D.高炉炼铁过程 中的还原剂主要是CO 中的还原剂主要是CO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
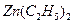 .
.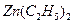 可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示该方法生成氧化锌的方法______。
可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示该方法生成氧化锌的方法______。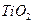 ) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分
) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分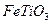 ),为原料按下过程进行的,请
),为原料按下过程进行的,请 完成下列化学方程式
完成下列化学方程式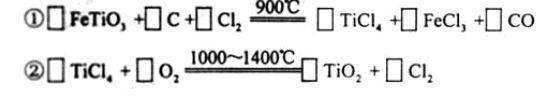
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) △H=-92.44 kJ/mol。其部分工艺流程如下图所示:
2NH3(g) △H=-92.44 kJ/mol。其部分工艺流程如下图所示: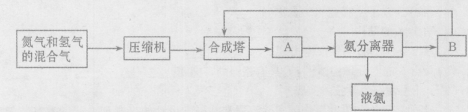
 ,阴极反应为 。
,阴极反应为 。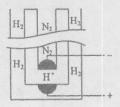
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com