
某研究小组在实验室用重晶石(主要成分BaSO4)对工业生产BaS进行模拟实验。BaS是可溶盐,在工业生产中,它是制备其他钡盐的中间产物。已知:
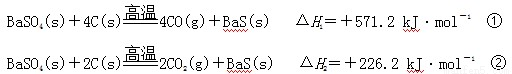
下列说法不正确的是
A.上述反应中BaSO4均作氧化剂
B.反应C(g)+CO2(g) 2CO(g)的ΔH3>+172.5 kJ·mol-1
2CO(g)的ΔH3>+172.5 kJ·mol-1
C.实际生产中必须加入过量的炭使BaSO4得到充分的还原,同时还要通入空气,因为①②为吸热反应,炭和氧气反应放热维持反应所需高温
D. 以BaS作为沉淀剂,用于铅和汞沉淀的转化
科目:高中化学 来源:2014高考名师推荐化学资源的综合应用(解析版) 题型:选择题
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是

A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子大量共存与推断(解析版) 题型:选择题
下列分子或离子在指定的分散系中能大量共存的一组是
A.银氨溶液: Na+、K+、NO3-、NH3·H2O
B.空气: C2H2、CO2、SO2、NO
C.氢氧化铁胶体: H+、K+、S2-、Br-
D.高锰酸钾溶液: H+、Na+、SO42-、葡萄糖分子
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学碳及其化合物主要性质(解析版) 题型:实验题
生铁中含碳和硫等元素。化学兴趣小组对某生铁样品进行了探究。根据要求回答下列问题。
Ⅰ.生铁中碳和硫元素的定性检验
按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验。
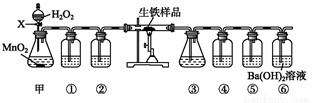
(1)仪器X的名称是 ;装置③⑤中试剂相同,装置④中盛放的试剂是 。(2)写出甲中反应的化学方程式 。(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在? ,理由是 。Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品w1 g进行实验,充分反应后,测得装置⑥中生成的沉淀为w2 g,该样品中碳的质量分数为 (用含w1、w2的式子表示)。(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果 (填“偏大”或“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学盖斯定律及其应用(解析版) 题型:填空题
(1)在焙烧炉中发生反应:
①Fe2O3(s)+3C(s) ===2Fe(s)+3CO(g) ΔH=-492.7 kJ·mol-1
②3CO(g)+Fe2O3(s) ===2Fe(s)+3CO2(g) ΔH=+25.2 kJ·mol-1
则2Fe2O3(s)+3C(s) ===4Fe(s)+3CO2(g) ΔH= kJ·mol-1。
(2)天然气(以甲烷计)在工业生产中用途广泛。甲烷蒸汽转化法制H2的主要转化反应如下:
CH4(g)+H2O(g) ===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+2H2O(g) ===CO2(g)+4H2(g) ΔH=+165.0 kJ·mol-1
上述反应所得原料气中的CO能使氨合成催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学盐类水解的概念与离子浓度大小比较(解析版) 题型:选择题
对滴有酚酞试液的下列溶液,操作后颜色变深的是
A.明矾溶液加热 B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl D.小苏打溶液中加入少量的NaCl固体
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学盐类水解的概念与离子浓度大小比较(解析版) 题型:选择题
W、X、Y、Z是原子序数依次增大的四种短周期元素,化合物WX能抑制水的电离。化合物Y2Z能促进水的电离,则Y元素是
A. Na B. F C. Li D. Cl
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学电解池的工作原理、电极反应式的书写(解析版) 题型:选择题
下列与装置有关的说法中正确的是
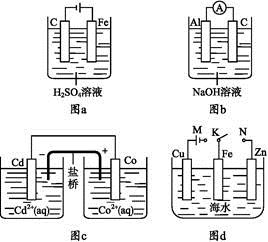
A.图a中,随着电解的进行溶液中H+的浓度越来越大
B.图b中,Al电极作电池的负极,电极反应为Al-3e- Al3+
Al3+
C.图c中,发生的反应为Co+Cd2+ Cd+Co2+
Cd+Co2+
D.图d中,K分别与M、N连接,Fe电极均受到保护不会腐蚀
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学物质的量及阿伏伽德罗常数(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是
A.在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2晶体中含有0.4NA个离子
D.铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com