
 ,a个-CH 3,其余为-OH,则该物质分子中-OH的个数可能为( )
,a个-CH 3,其余为-OH,则该物质分子中-OH的个数可能为( )| A. | m-a | B. | n+m+a | C. | m+1-a | D. | m-1-a |
分析 有机物主要靠C原子连接,每个碳原子都必须形成4个共价键,以1条碳链分析考虑,先分析若只连接甲基,计算连接的甲基数目,再根据分子中含有的甲基数目计算羟基数.1个 可连接1个甲基,-CH2-不管多少个只能连接两个-CH3.据此计算判断.
可连接1个甲基,-CH2-不管多少个只能连接两个-CH3.据此计算判断.
解答 解:①若形成的有机物为链状结构,假设只连接甲基,-CH2-不管多少个只能连接两个-CH3,m个 ,能连接m个-CH3,所以n个-CH2-,m个-CH-,连接-CH3共计m+2个.由于分子中含有a个-CH3,所以连接的-OH为m+2-a;
,能连接m个-CH3,所以n个-CH2-,m个-CH-,连接-CH3共计m+2个.由于分子中含有a个-CH3,所以连接的-OH为m+2-a;
②若形成的有机物为环状结构,则不管-CH2-是多少个,均不能连甲基,而m个 能连m个甲基,故共能连甲基m个,但由于分子中含有a个-CH3,所以连接的-OH为m-a;
能连m个甲基,故共能连甲基m个,但由于分子中含有a个-CH3,所以连接的-OH为m-a;
故选A.
点评 本题考查常见有机物结构,侧重考查学生知识迁移能力,采用补缺法分析解答即可,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
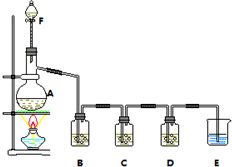 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
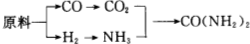

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 0.1 mol/L的Na2CO3溶液中加入0.01 molCH3COOH:CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4 mol/L的NaAlO2溶液和7 mol/L的盐酸等体积均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 向HCOOK和KOH的混合溶液中加入KMnO42KMnO4+HCOOK+KOH═2K2MnO4+CO2↑+H2O | |
| D. | 在含有Mn2+的溶液中加入HNO3再加入PbO2,则反应体系显紫红色:5PbO2+2Mn2++4H+═5Pb2++2MnO4-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | lmol该有机物可消耗3mol NaOH | B. | 该有机物的分子式为C16H1705 | ||
| C. | 最多可与7molH2发生加成 | D. | 苯环上的一溴代物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
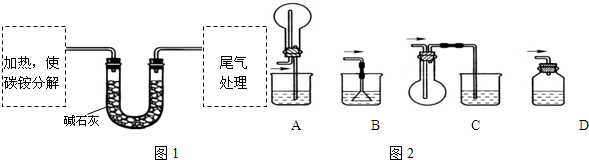
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com