
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
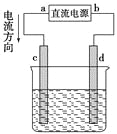
A. a为负极,b为正极
B. a为阳极,b为阴极
C. 电解过程中,d电极质量增加
D. 电解过程中,氯离子浓度不变
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】已知土壤胶体带负电,在土壤里施用含氮量相等的下列肥料,肥效较差的是( )
A.(NH4)2SO4
B.NH4HCO3
C.NH4NO3
D.NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是氧族部分元素的相关性质。
元素 性质 | 8O | 16S | 34Se | 52Te |
主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
原子半径 | 逐渐增大 | |||
单质与H2 反应情况 | 点燃时 易化合 | 加热 化合 | 加热 难化合 | 不能 直接化合 |
请回答下列问题:
(1)硒在周期表中位置____。
(2)碲的化合价可能有____。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是__________(填化学式)。
(4)氢硒酸有较强的____(填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_____________。
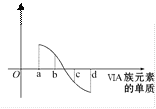
(5)氧族元素单质与H2反应过程中的焓变如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表___,d代表___(均写单质名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 试管内壁附着的硫可用二硫化碳溶解除去
B. 单质硫既有氧化性,又有还原性
C. 硫在空气中燃烧的产物是二氧化硫
D. 硫在过量纯氧中燃烧的产物是三氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: 
(1)地壳中含量最高的金属元素在周期表中的位置是 .
(2)⑧形成的单质与水反应的离子方程为 .
(3)②⑦的非金属性强弱可通过比较这两种元素(填编号)
a.原子的得电子的能力 b.含氧酸的酸性
c.气态氢化物的稳定性 d.单质的熔沸点
(4)写出一种由④⑤⑧元素形成的既含有离子键又含有共价键的物质的电子式 .
(5)化工行业最近合成了由元素②和③形成的化合物,其硬度比金刚石还大.该物质所形成的晶体还可能具有的性质或特点有(填编号)
①熔点很高 ②可以导电 ③不存在单个分子 ④具有空间网状结构
(6)①和③形成的某液态化合物摩尔质量与氧气相同.在常温常压下0.25mol该液态物质在足量的氧气中完全燃烧生成③的气态单质和液态水,同时放出QkJ的热量.写出该反应的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe与稀HNO3反应时,若两者消耗物质的量之比为4:10,且生成Fe(NO3)2,则反应中生成的还原产物可能是( )
A.N2B.N2OC.NOD.N2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以玉米淀粉为原料生产燃料乙醇的生产过程可由下图表示:
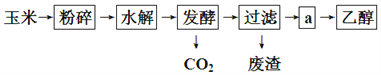
(1)乙醇分子中所含的官能团的名称为:__________________;
(2)过滤后得到a的主要成分为葡萄糖和乙醇,步骤a的操作是__________;
A.蒸发 B.萃取 C.蒸馏 D.分液
(3)生产过程中为了检验水解是否开始,可使用的试剂是______________;
(4)已知1g乙醇完全燃烧放出的热量为29.7kJ,请据此写出乙醇燃烧的热化学方程式:_______。
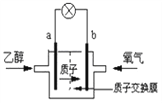
(5)为了充分利用乙醇的能量,科学家还把乙醇设计成燃料电池,如图,用磺酸类质子溶剂,在高温供电时,乙醇电池效率高且更安全。请判断,该电池的a极为电池的_______极(填“正”或“负”),b极的电极反应式为:____________________________,电池工作时,若有1mol乙醇被氧化,则转移的电子为____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质反应时,改变反应条件或者反应物的物质的量之比,生成的产物不变的是( )
A.Na与氧气 B.澄清石灰水与二氧化碳
C.氯化铝溶液与氢氧化钠溶液 D.Al与稀盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com